
| A. | c(N2):c(H2):c(NH3)=1:3:2 | |
| B. | 2v(H2)=3v(NH3) | |
| C. | 单位时间内1个N≡N键断裂的同时,有6个N-H键断裂 | |
| D. | 单位时间消耗0.1molN2的同时,生成0.2molNH3 |
分析 根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:A、c(N2):c(H2):c(NH3)=1:3:2,并不能说明浓度不变,所以不一定是平衡状态,故A错误;
B、未体现正与逆的关系,故B错误;
C、单位时间内1个N≡N键断裂,等效于6个N-H键形成,同时有6个N-H键断裂,所以正逆反应速率相等,反应达平衡状态,故C正确;
D、只要反应发生就符合单位时间消耗0.1molN2的同时,生成0.2molNH3,故D错误;
故选C.
点评 本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.


科目:高中化学 来源: 题型:选择题
| A. | 已知①Fe(s)+$\frac{1}{2}$O2(g)═FeO(s)△H1=-272 kJ/mol;②2Al(s)+$\frac{3}{2}$O2(g)═Al2O3(s)△H2=-1675kJ/mol,则2Al(s)+3FeO(s)=Al2O3(s)+3Fe(s);△H=-859 kJ/mol | |
| B. | 25℃时,向10mL物质的量浓度均为0.10mol/LNaOH和NH3•H2O的混合溶液中,逐滴滴加 10mL0.10mol/L 盐酸,混合溶液中 c(NH4+)+c(H+)=c(OH-) | |
| C. | 25℃时,向0.10mol/LNaHSO3溶液中通入NH3至溶液PH=7(体积变化忽略),则有:c(Na+)>c(NH4+)>c(SO32-) | |
| D. | 比较Na2S2O3溶液与不同浓度稀硫酸反应速率的快慢是通过测定出现黄色沉淀的快慢来比较的,而不是采用排水法测量单位时间内气体体积的大小进行比较的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{92}^{235}U$是核电站的主要原料,2.35g${\;}_{92}^{235}U$的中子数为0.92NA | |
| B. | ${\;}_{53}^{131}I$具有放射性,1.31g${\;}_{53}^{131}I$具有的中子数为0.78NA | |
| C. | 标准状况下,11.2L氦气中约含有NA个氦原子 | |
| D. | 0.1mol•L-1Na2CO3溶液中含有0.1NA个CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 容器编号 | 温度(℃) | |||
| 起始物质的量(mol) | 平衡物质的量(mol) | |||
| CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
| Ⅰ | 387 | 0.20 | 0.080 | 0.080 |
| Ⅱ | 387 | 0.40 | ||
| Ⅲ | 207 | 0.20 | 0.090 | 0.090 |
| A. | 该反应的逆反应为放热反应 | |
| B. | 达到平衡时,容器Ⅰ中的CH3OH体积分数比容器Ⅱ中的小 | |
| C. | 达到平衡时,容器Ⅰ中的压强与容器Ⅲ中的压强相同 | |
| D. | 若起始时向容器Ⅰ中充入CH3OH 0.15 mol、CH3OCH3 0.15 mol 和H2O 0.10 mol,则反应将向正反应方向进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 尿素是首个由无机物人工合成的有机物.工业上尿素由CO2和NH3在一定条件下合成,当氨碳比n(NH3)/n(CO2)=4,CO2的转化率随时间的变化关系如图所示,则A点的逆反应速率v逆(CO2)与B点的正反应速率v正(CO2)的大小关系为( )
尿素是首个由无机物人工合成的有机物.工业上尿素由CO2和NH3在一定条件下合成,当氨碳比n(NH3)/n(CO2)=4,CO2的转化率随时间的变化关系如图所示,则A点的逆反应速率v逆(CO2)与B点的正反应速率v正(CO2)的大小关系为( )| A. | v逆(CO2)>v正(CO2) | B. | v逆(CO2)<v正(CO2) | C. | v逆(CO2)=v正(CO2) | D. | 无法判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验序号 | 时间 浓度 温度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | c3 | 0.92 | 0.75 | 0.60 | 0.60 | 0.60 | 0.60 |
| 4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 如图所示的装置在实验室中用途比较广泛:
如图所示的装置在实验室中用途比较广泛:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
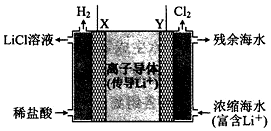 浓差电池中的电动势是由于电池中存在浓度差而产生的.某浓差电池的原理如图所示,该电池从浓缩海水中提取LiCl的同时又获得了电能.下列有关该电池的说法错误的是( )
浓差电池中的电动势是由于电池中存在浓度差而产生的.某浓差电池的原理如图所示,该电池从浓缩海水中提取LiCl的同时又获得了电能.下列有关该电池的说法错误的是( )| A. | 电池工作时,Li+通过离子电子导体移向b区 | |
| B. | 电流由X极通过外电路移向Y极 | |
| C. | 正极发生的反应为:2H++2e-=H2↑ | |
| D. | Y极每生成1 mol Cl2,a区得到2 mol LiCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将pH均为a的氢氧化钠溶液和氨水分别加水稀释100倍,pH变为b和c,则a、b、c的大小关系是:b>c>a | |
| B. | 常温下5.0×10-3mol•L-1KHA溶液的pH=3.75,该溶液中c(A2-)<c(H2A) | |
| C. | 室温时,M(OH)2(s)?M2+(aq)+2OH-(aq) Ksp=a; c(M2+)=b mol•L-1时,溶液的pH等于14 | |
| D. | Na2C2O4溶液:c(OH-)=c(H+)+c(HC2O4-)+2c(H2C2O4) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com