
分析 将6mol H2和3mol CO充入容积为1L的密闭容器中,2秒末时,经测定,容器内 CH3OH(g)有2.1mol,则:
2H2(g)+CO(g)?CH3OH(g)
起始量(mol):6 3 0
变化量(mol):4.2 2.1 2.1
2s末时(mol):1.8 0.9 2.1
(1)根据v=$\frac{△c}{△t}$计算H2的反应速率;
(2)转化率=$\frac{物质的量变化量}{起始物质的量}$×100%.
解答 解:将6mol H2和3mol CO充入容积为1L的密闭容器中,2秒末时,经测定,容器内 CH3OH(g)有2.1mol,则:
2H2(g)+CO(g)?CH3OH(g)
起始量(mol):6 3 0
变化量(mol):4.2 2.1 2.1
2s末时(mol):1.8 0.9 2.1
(1)2s内H2的反应速率为$\frac{\frac{4.2mol}{1L}}{2s}$=2.1mol/(L.min),
答:2s内H2的反应速率为2.1mol/(L.min);
(2)CO的转化率=$\frac{2.1mol}{3mol}$×100%=70%,
答:CO的转化率为70%.
点评 本题考查化学平衡计算,比较基础,理解掌握三段式在化学平衡计算应用.


 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
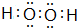 该物质能使酸性KMnO4溶液褪色,在这个反应中体现了该物质的还原性(填“氧化性”或“还原性”)
该物质能使酸性KMnO4溶液褪色,在这个反应中体现了该物质的还原性(填“氧化性”或“还原性”)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原溶液中氨水中的c(OH-)与醋酸中的c(H+)相等 | |
| B. | CH3COONH4不发生分解 | |
| C. | 混合溶液中,c(NH3•H2O)=c(CH3COOH) | |
| D. | Kb(NH3•H2O)=3Ka(CH3COOH) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4 mol | B. | 3.4 mol | C. | 2.8 mol | D. | 1.2 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(O2)/mol | 0.7 | 0.4 | 0.3 | x | x | x |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| t/min | X/mol | Y/mol | Z/mol |
| 0 | 1.00 | 1.00 | 0.00 |
| 1 | 0.90 | 0.80 | 0.20 |
| 3 | 0.75 | 0.50 | 0.50 |
| 5 | 0.65 | 0.30 | 0.70 |
| 9 | 0.55 | 0.10 | 0.90 |
| 10 | 0.55 | 0.10 | 0.90 |
| 14 | 0.55 | 0.10 | 0.90 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 实验室配制500mL 0.2mol•L-1的Na2SO4溶液,实验操作步骤有:
实验室配制500mL 0.2mol•L-1的Na2SO4溶液,实验操作步骤有:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠是淡黄色固体 | |
| B. | 钠的密度:小于煤油大于水 | |
| C. | 钠在化学反应中只能做还原剂 | |
| D. | 钠与硫酸铜溶液反应有红色的铜生成 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com