
����Ŀ����14�֣�ij�����������̿���п����Ҫ�ɷ�ΪMnO2��ZnS�����������FeS��CuS��Al2O3�����ʣ�Ϊԭ����ȡZn��MnO2��
��1����һ�������£��������ֿ����������Һ������ã���ƽ���µĻ�ѧ����ʽ��
MnO2 + FeS + H2SO4![]() MnSO4 + Fe2(SO4)3 + S + H2O
MnSO4 + Fe2(SO4)3 + S + H2O
��2�������ú���Mn2+��Fe3+��Cu2+��Al3+��Zn2+��������Һ�����µĹ�ҵ���̽��в�����������Һ��IV���������Һ��IV������MnO2��Zn��
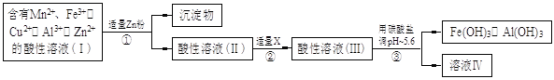
a���������м�Zn�ۺ�����Ӧ�����ӷ���ʽΪ ��
b���������м�������X��������ʲô ��X����ѡ��Ļ�ѧʽ�� ��
c��������������̼���εĻ�ѧʽ�� ��
��3��Ϊ�˴����������в�����Fe(OH)3��Al(OH)3����������л���Al(OH)3��������������µ��й�����ͼ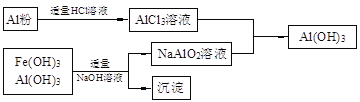
a��AlCl3��Һ��NaAlO2��Һ��Ӧ����AI(OH)3�����ӷ���ʽΪ �����ܹ��õ�n molAl(OH)3�������ĵ�NaOH��HCl����������mol���ֱ�Ϊ �� ��
b����ʹ���������̻��մ�������Ƚ�����������������������
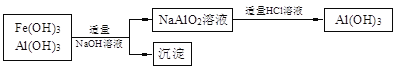
���𰸡���1��3 MnO2 + 2 FeS + 6H2SO4== 3 MnSO4 + 1 Fe2(SO4)3 + 2 S + 6 H2O (2��)
��2��a��Zn + 2Fe3+==Zn2+ + 2Fe2+��Zn + Cu2+==Zn2+ + Cu (2��)
b����Fe2+������Fe3+MnO2(2��)
c��MnCO3��ZnCO3��MnCO3��ZnCO3(2��)
��3��a��Al3++ 3AlO2��+ 6H2O==4Al(OH)3�� (2��)![]()
![]() (2��)
(2��)
b���簴�����̣���õ�ͬ��n molAl(OH)3�����ĵ�NaOH��HCl���������ֱ�Ϊn mol������ǰ���̵�����������Զ��ԣ�ǰ���̸����Ͻ�Լ��ԭ��(2��)
�������������������1����һ�������£��������ֿ����������Һ������ã�����ԭ���غ㡢�����غ�ɵ���ƽ�Ļ�ѧ����ʽ��3MnO2 + 2FeS +6H2SO4==3MnSO4 + Fe2(SO4)3 +2S + 6H2O��a�������������Һ�м���Zn�ۺ���Һ�е�Fe3+��Cu2+����Zn����������ԭ��Ӧ��������Ӧ�����ӷ���ʽΪZn + 2Fe3+==Zn2+ + 2Fe2+��Zn + Cu2+==Zn2+ + Cu������ͼʾ��֪��������Һ���к���Fe2+��Al3+�ȣ�Ҫ�����Ƿ�Ӧת��ΪAl(OH)3��Fe(OH)3������Ӧ���ȼ���������������Һ�е�Fe2+����ΪFe3+��Ϊ�˲������µ��������ӣ������������������MnO2��c��������������̼���ξ��ǵ�����Һ������Եģ����ݳ��ӵ�ԭ������Ӧ���ǵĻ�ѧʽ��MnCO3��ZnCO3����3��a��AlCl3��Һ��NaAlO2��Һ��Ϸ����ε�˫ˮ�ⷴӦ����AI(OH)3���÷�Ӧ�����ӷ���ʽΪAl3++ 3AlO2��+ 6H2O==4Al(OH)3��������n(Al3+)��n(AlO2��)=1:3,�������ܹ��õ�n molAl(OH)3������Ҫ����AlCl3�����ʵ�����n/4mol������NaAlO2�����ʵ�����3n/4mol������Ԫ���غ��֪n(NaOH)=n(NaAlO2)= 3n/4mol��n(HCl)=3n(AlCl3)= 3n/4mol��b����ʹ���������̻��մ������õ�ͬ��n molAl(OH)3�����ĵ�NaOH��HCl���������ֱ�Ϊn mol������ǰһ�������������������������Զ��ԣ�ǰ���̸����Ͻ�Լ��ԭ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±�ΪԪ�����ڱ���һ���֣�
̼ | �� | Y | |
X | �� | Z |
��ش���������:
��1��ZԪ�������ڱ��е�λ��Ϊ________________��
��2������Ԫ��ԭ�Ӱ뾶�����ǣ�дԪ�ط��ţ�________________��
��3��������ʵ��˵��YԪ�صķǽ����Ա���Ԫ�صķǽ�����ǿ����________������ţ���
a��Y������H2S��Һ��Ӧ����Һ�����
b����������ԭ��Ӧ�У�1molY���ʱ�1mol��õ��Ӷ�
c��Y������Ԫ�صļ��⻯�����ȷֽ⣬ǰ�ߵķֽ��¶ȸ�
��4������һ������ͭ��һ��Ũ�ȵ����������Ļ���ᷴӦ�����ɵ���ֻ������ͭ��ͬʱ���ɵ�������������ϱ�������Ԫ����ɣ��������Է���������С��50��Ϊ��ֹ��Ⱦ����������������ȫת��Ϊ��ۺ������Σ�����1L2.2mol��L��1 NaOH��Һ��1molO2������������ķ���ʽ�����ʵ����ֱ�Ϊ______________________________����������ͭ���ʵ���Ϊ_______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Һ���ܴ�����������ҺΪ��ɫ�����������ǣ� ��
A. K+ ��MnO4����Na+��Cl�� B. K+��Mg2+��NO3����Cl��
C. Na+��OH����NH4+��CO32�� D. Fe3+��Na+��Cl����SO42��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ܶ��ʻ���ˮ������ζ���������Ļ�����ͼ��ͼ1����ϩ��Ϊԭ����ȡ���������Ĺ��̣����ֲ���ͷ�Ӧ��������ȥ���� 
��ش��������⣺
��1��B�Ľṹ��ʽΪ ��
��2����ϩ��ˮ��Ӧ����A�ķ�Ӧ����Ϊ ��
��3��A��C��Ӧ�������������Ļ�ѧ����ʽΪ �� �䷴Ӧ����Ϊ ��
��4��ʵ���ҿ���ͼ2װ����ȡ���������� �����Թ�a�мӺ�����Լ�����Ҫ����2��3������Ƭ���������� ��
���Թ�b��ʢ�б���̼������Һ�����ɵ����������ڸ���Һ������ϡ����¡����㣬�÷�Һ�ķ���������ò�Ʒ�������Ҫ������ �� �Թ�b�еĵ��ܿ�Ӧ��Һ���Ϸ��������뵽Һ�����£���ԭ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ݲ⣬����������̼������ͬλ��12C��13C��ԭ�Ӹ���֮��Ϊ65:1����������12C��13C��ԭ�Ӹ���֮��Ϊ89��1�� ������̼Ԫ�ص����ԭ�������� 12.011����ô����������̼Ԫ�ص����ԭ������Ӧ�� ������ ��
A.12.000B.12.009
C.12.015D.12.005
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��NaCl��MgSO4���ܽ�����ߣ�����˵����ȷ���ǣ� �� 
A.ֻ����t1��ʱ��NaCl��MgSO4���ܽ�Ȳ����
B.t1�桫t2�棬MgSO4���ܽ�����¶����߶���С
C.��t2��ʱ��MgSO4������Һ�����������������
D.��MgSO4������Һ���¶ȴ�t3�潵��t2��ʱ���о�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ȼ�ŵ�����ͷ��̻�������һЩ������������Ϊ�̻��ķ�ɫ�������н����������У���ɫ��Ӧ����ɫ����
A.NaClB.K2CO3C.CaCl2D.CuCl2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ֶ���������Ԫ��W��X��Y��Z��ԭ��������������W��X�ļ����Ӿ�����ͬ���Ӳ�ṹ��X��ԭ�Ӱ뾶�Ƕ���������Ԫ��ԭ�������ģ�W�� Yͬ����Z ��X �γɵ����ӻ������ˮ��Һ�����ԡ�����˵����ȷ����
A. �����Ӱ뾶��W<X<Z
B. W��X�γɵĻ���������ˮ����Һ�ʼ���
C. ��̬�⻯������ȶ��ԣ�W<Y
D. ����������ˮ��������ԣ�Y>Z
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Դ�ǽ��������Ⱦ����Ҫ�ٴ룬���м״����Ҵ������鶼�����ʵ����ȼ�ϣ�������ȼ�ϵ�ء�
��1����֪����C2H5OH(l)��3O2(g)��2CO2(g)��3H2O(g) ��H1����1366.8kJ/mol
��2CO(g)��O2(g)��2CO2(g) ��H2����566.0kJ/mol
��H2O(g)��H2O(l) ��H3����44 kJ/mol��
�Ҵ�����ȫȼ������һ����̼��Һ̬ˮ���Ȼ�ѧ����ʽΪ��______________________��
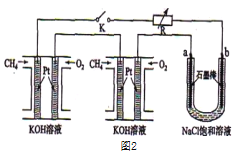
��2�������ü״�ȼ�շ�Ӧ���һ��ȼ�ϵ�ء�����ͼ1����Pt���缫���ϣ�������������Һ���������Һ���������缫�Ϸֱ����״���������
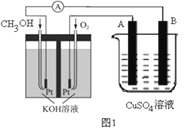
��д��ȼ�ϵ�ظ����ĵ缫��Ӧʽ_________________��
�������ø�ȼ�ϵ���ṩ��Դ����ͼ1�ұ��ձ������������������ͭ��������Ӧ��_______��(����A������B��)������������������6.4gʱ��ȼ�ϵ�������������ı�״�������Ϊ________L��
��3��ij�о�С�齫��������ȼ�ϵ�ش���������ͼ2��Ϊ��Դ�����б����Ȼ�����Һ���ʵ����ÿ����ؼ���ͨ����Ϊ1 L(��״��)���ҷ�Ӧ��ȫ����������ͨ�����صĵ�������ʽΪ_____________(�����ڳ���F��9.65��l04C/ mol)������ܲ������������Ϊ_____L(��״��)��
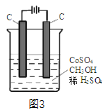
��4����ⷨ�������״���ˮ����ɵ���Ⱦ��ԭ���ǣ�ͨ�罫Co2+������������Co3+�����ɵ�Co3+���״�������CO2��H+(��ʯīϩ��ȥCo2+)��������ͼ3��ʾװ��ģ���������̣���Co2+�������ĵ缫��ӦʽΪ________________________��ȥ�״������ӷ���ʽΪ______________________________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com