
| A | B | C | D |
 |  |  |  |
| 验证化学能转化为电能 | 验证非金属性:Cl>C>Si | 实验室制氨气 | 研究催化剂对化学反应速率的影响 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.没有构成闭合回路;
B.盐酸易挥发,盐酸与硅酸钠溶液反应;
C.氯化铵分解后,在试管口又化合生成氯化铵;
D.由控制变量研究反应速率的影响因素可知,只有一个变量.
解答 解:A.没有构成闭合回路,不能形成原电池装置,则不能验证化学能转化为电能,故A错误;
B.盐酸易挥发,盐酸与硅酸钠溶液反应,则不能比较C、Si的非金属性,故B错误;
C.氯化铵分解后,在试管口又化合生成氯化铵,不能制备氨气,应利用铵盐与碱加热制备,故C错误;
D.由控制变量研究反应速率的影响因素可知,只有一个变量催化剂,则图中装置可研究催化剂对化学反应速率的影响,故D正确;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,把握原电池、酸性比较、气体的制备、反应速率影响因素等为解答的关键,侧重分析与实验能力的考查,注意相关反应原理及实验装置的作用、实验评价性分析,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 每个53131Cs含有78个中子 | B. | CsOH的碱性比KOH的强 | ||
| C. | HI的还原性比HF的强 | D. | KIO3是碘的最高价含氧酸的盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
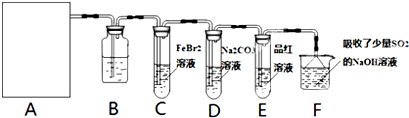
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
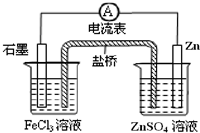 根据下列原电池示意图,回答下列问题:
根据下列原电池示意图,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
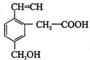 某机物的结构如图所示,这种有机物不可能具有的性质是( )
某机物的结构如图所示,这种有机物不可能具有的性质是( )| A. | ①④ | B. | ②⑤ | C. | ②⑥ | D. | 只有⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

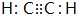 ;D的最简式CH2;
;D的最简式CH2; +Br2 $\stackrel{FeBr_{3}}{→}$
+Br2 $\stackrel{FeBr_{3}}{→}$ +HBr,其反应类型为取代反应.
+HBr,其反应类型为取代反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯的结构简式可表示为CH2CH2 | B. | 乙醇的分子式:CH3CH2OH | ||
| C. | 甲烷的结构式:CH4 | D. | 甲苯的键线式可表示为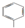 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
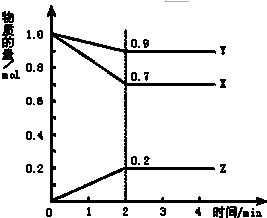 某温度时,在2L容器中X、Y、Z三种物质随时间的变化曲线如图所示,由图中的数据分析,反应开始至2min时:
某温度时,在2L容器中X、Y、Z三种物质随时间的变化曲线如图所示,由图中的数据分析,反应开始至2min时:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com