
X、Y、Z、W、R五种短周期非金属主族元素在元素周期表中的位置如图所示,下列有关说法正确的是( )
| X | Y | ||
| Z | W | R |
A.Z位于第三周期ⅤA族
B.X、Y的气态氢化物的稳定性:X>Y
C.原子半径大小顺序:Z>W>Y
D.W、R的最高价氧化物对应水化物的酸性:W>R
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:
有人设计以Pt和Zn为电极材料,埋入人体内作为某种心脏病人的心脏起搏器的能源。它依靠跟人体内体液中含有的一定浓度的溶解氧、H+和Zn2+进行工作,试写出该电池的两极反应式。
查看答案和解析>>
科目:高中化学 来源: 题型:
标准状况下,气态分子断开1mol化学键的焓变称为键焓。已知H—H,H—O,和O==O键的键焓△H分别为436KJ/mol,463KJ/mol,495KJ/mol,下列热化学方程式正确的是( )
A、H2O(g)==H2(g)+1/2O2( g) △H =—485KJ/mol
g) △H =—485KJ/mol
B、H2O(g)==H2(g)+1/2O2(g) △H = + 485KJ/mol
C、2 H2(g) + O2(g)==2 H2O(g) △H = + 485KJ/mol
D、2 H2(g) + O2(g)==2 H2O(g) △H =—485KJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
甲醇是人们开发和利用的一种新能 源。已知:
源。已知:
①2H2(g)+O2(g)===2H2O(l)
ΔH1=-571.8 kJ·mol-1;
②CH3O H(g)+1/2O2(g)===CO2(g)+2H2(g)
H(g)+1/2O2(g)===CO2(g)+2H2(g)
ΔH2=-192.9 kJ·mol-1
(1)甲醇蒸气完全燃烧的热 化学方程式为______________________________________。
化学方程式为______________________________________。
(2)反应②中的能量变化如图所示,则ΔH2=________。
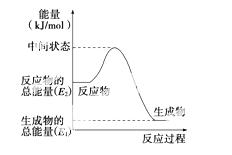
(3)H2(g)的燃烧热为________。
(4)请你分 析H2(g)作为能源比甲醇蒸气作为能源的优点:
析H2(g)作为能源比甲醇蒸气作为能源的优点:
__________________________________________________
__________________________________________________(写出两点即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
元素周期表和元素周期律可以指导人们进行规律性的推测和判断。下列说法不合理的是( )
A.若X+和Y2-的核外电子层结构相同,则原子序数:X>Y
B.由水溶液的酸性:HCl>H2S,可推断元素的非金属性:Cl>S
C.硅、锗都位于金属与非金属的交界处,都可以作半导体材料
D.Cs和Ba分别位于第六周期ⅠA和ⅡA族,则碱性:CsOH>Ba(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W代表短周期的四种元素,有关它们的部分结构及性质信息如下表所示。
| 元素 | 部分结构信息 | 部分性质信息 |
| X | X的单质由双原子分子构成,分子中有14个电子 | X有多种氧化物,如XO、XO2、X2O4等;通常情况下XO2与X2O4共存 |
| Y | Y原子的次外层电子数等于最外层电子数的一半 | Y能形成多种气态氢化物 |
| Z | Z原子的最外层电子数多于4 | Z元素的最高正化合价与最低负化合价代数和等于6 |
| W | W原子的最外层电子数等于2n-3(n为原子核外电子层数) | 化学反应中W原子易失去最外层电子形成Wn+ |
请按要求回答下列问题(注意不能用字母X、Y、Z、W作答):
(1)X的气态氢化物分子的电子式是________________________,Z元素在周期表中的位置是________。
(2)X、Y、Z三元素的最高价氧化物对应水化物的酸性由强到弱的顺序是__________________________________________________。
(3)常温时,W的硫酸盐溶液的pH________7(填“<”、“>”或“=”),理由是__________________________________________________________
_____________________________________________ (用离子方程式表示)。
(4)实验室用X的氢化物的水溶液制取W的氢氧化物的方法是(用离子方程式表示)______________________________________________。
(5)25 ℃、101 kPa时,32 g Y的最低价气态氢化物完全燃烧生成稳定的氧化物时放出1 780.6 kJ的热量,写出该反应的热化学方程式:_______
______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
N2O5是一种新型硝化剂,在一定温度下可发生以下反应:
2N2O5(g)  4NO2 (g)+ O2(g) ΔH > 0,t℃时,向密闭容器中通入N2O5,部分实验数据见下表:
4NO2 (g)+ O2(g) ΔH > 0,t℃时,向密闭容器中通入N2O5,部分实验数据见下表:
| 时间/s | 0 | 500 | 1000 | 1500 |
| c(N2O5)/ mol·L-1 | 5.00 | 3.52 | 2.50 | 2.50 |
下列说法中不正确的是 ( )
A.500 s 内N2O5分解速率为2.96×10-3mol·L-1·s-1
B.达平衡时,N2O5的转化率为50%
C.达平衡后,升高温度平衡常数减小
D.达平衡后其他条件不变,将容器体积压缩到原来的一半,c(N2O5)> 5.00 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
某烷烃相对分子质量为86,如果分子中含有3个—CH3、
2个—CH2—和1个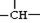 ,则该结构的烃的一氯取代物最多可能有( )种(不考虑立体异构)
,则该结构的烃的一氯取代物最多可能有( )种(不考虑立体异构)
A.4 B.5 C.6 D.9
查看答案和解析>>
科目:高中化学 来源: 题型:
用惰性电极电解M(NO3)x的水溶液,当阴极上增重a g时,在阳极上同时产生b L 氧气(标准状况),从而可推知M的相对原子质量为( )
氧气(标准状况),从而可推知M的相对原子质量为( )
A.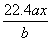 B.
B.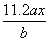
C.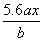 D.
D.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com