
分析 NO具有强的还原性,空气中容易被氧化为二氧化氮;氯气与水反应生成的次氯酸具有强的氧化性,能够杀菌消毒;向下排空气法收集的气体其密度应小于空气密度;氯气与水反应生成的氯化氢和二氧化氮与水生成的硝酸为强酸.
解答 解:NO为无色气体,具有强的还原性,空气中容易被氧化为二氧化氮,二氧化氮为红棕色;
氯气与水反应生成的次氯酸具有强的氧化性,能够杀菌消毒,常用于自来水杀菌、消毒;
向下排空气法收集的气体其密度应小于空气密度,符合条件的气体为氨气;
氯气与水反应生成的氯化氢和二氧化氮与水生成的硝酸为强酸;
故答案为:NO;Cl2;NH3;Cl2和NO2.
点评 本题考查较综合,侧重物质性质的考查,熟悉常见物质之间的反应即可解答,注重基础知识的考查,题目较简单.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
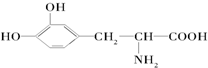 .这种药物的研制是基于获得2000年诺贝尔生理学和医学奖的研究结果.L多巴分子中不含有的官能团是( )
.这种药物的研制是基于获得2000年诺贝尔生理学和医学奖的研究结果.L多巴分子中不含有的官能团是( )| A. | 羟基 | B. | 氨基 | C. | 羧基 | D. | 醛基 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
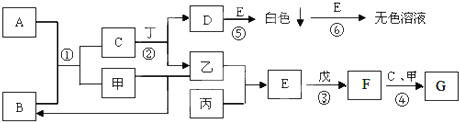
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | V3>V1=V2 | B. | V3=V2>V1 | C. | V3>V2>V1 | D. | V1=V2>V3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.02 mol/L | B. | 0.05 mol/L | C. | 1 mol/L | D. | 2mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯水的颜色呈浅黄绿色,说明氯水中含有Cl2 | |
| B. | 向氯水中滴加硝酸酸化的AgNO3溶液,产生白色沉淀,说明氯水中含有Cl- | |
| C. | 向氯水中加入NaHCO3粉末;有气泡产生,说明氯水中含有H+ | |
| D. | 氯水中加入氢氧化钠溶液,氯水的黄绿色消失,说明氯水中含有HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

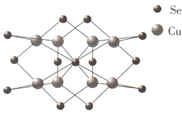
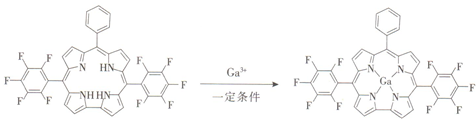
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀盐酸与稀氨水反应:H++OH-═H2O | |
| B. | 溴化钠溶液与氯气反应:2Br-+Cl2=═Br2+2Cl- | |
| C. | 碳酸钙与醋酸反应:CaCO3+2H+═Ca2++CO2↑+H2O | |
| D. | 二氧化氮与水反应:2NO2+2H2O═2H++2NO${\;}_{3}^{-}$+H2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com