
【题目】某同学按下列步骤配制100mL0.200molL﹣1Na2CO3溶液,请回答有关问题.实验步骤有关问题
【答案】2.12g|分析天平或电子天平|用玻璃棒搅拌|冷却至室温|100mL容量瓶|用玻璃棒引流|加蒸馏水至容量瓶中的液面接近刻度线1﹣2cm处,改用胶头滴管滴加至溶液的凹液面正好与刻度线相|切贴标签|不是|因为该同学没有洗涤烧杯和玻璃棒
【解析】解:(1)配制100mL0.200molL﹣1Na2CO3溶液,需要溶质碳酸钠的质量m=0.200mol/L×0.1L×106g/mol=2.12g;所以答案是:2.12g;(2)托盘天平精确度为0.1g;要想精确度达到0.01g,应选择分析天平或电子天平;所以答案是:分析天平或电子天平;(3)为了加快溶解速率,常采取的措施:用玻璃棒搅拌;所以答案是:用玻璃棒搅拌;(4)容量瓶为精密仪器,不能盛放过热、过冷液体,移液时应冷却到室温,配制100mL溶液应选择100mL容量瓶,容量瓶瓶颈较细,移液时为防止溶液溅出,应采取的措施是用玻璃棒引流;所以答案是:①冷却至室温;②100mL容量瓶;③用玻璃棒引流;(5)定容时,开始直接加蒸馏水至容量瓶中的液面接近刻度线1﹣2cm处,改用胶头滴管滴加至溶液的凹液面正好与刻度线相切;所以答案是:加蒸馏水至容量瓶中的液面接近刻度线1﹣2cm处,改用胶头滴管滴加至溶液的凹液面正好与刻度线相切;(6)配制一定物质的量浓度溶液一般步骤:计算、称量、溶解、冷却、移液、定容、摇匀、贴标签;所以答案是:贴标签;该实验漏掉洗涤操作,导致部分溶质损耗,溶质的物质的量偏小,依据C= ![]() 可知,最终配制溶液的浓度小于0.200molL﹣1;所以答案是:不是;因为该同学没有洗涤烧杯和玻璃棒;
可知,最终配制溶液的浓度小于0.200molL﹣1;所以答案是:不是;因为该同学没有洗涤烧杯和玻璃棒;


科目:高中化学 来源: 题型:
【题目】下列反应中,属非氧化还原反应的是
A. 3CuS+8HNO3==3Cu(NO3)2+2NO↑+3S↓+4H2O
B. 3Cl2+6KOH == 5KCl+KClO3+3H2O
C. 3H2O2+2KCrO2+2KOH==2K2CrO4+4H2O
D. 3CCl4+K2Cr2O7==2CrO2Cl2+3COCl2+2KCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相对分子质量不超过100的有机物A,既能与金属钠反应产生无色气体,又能与碳酸钠反应产生无色气体,还可以使溴的四氯化碳溶液褪色。 A完全燃烧只生成CO2和H2O。经分析其含氧元素的质量分数为37.21%。
① 其A的相对分子质量为________________
② A的实验式为_____________
③经核磁共振检测发现A的氢谱图如下,写出A的结构简式:_____________

④试写出A与甲醇反应的化学反应方程式:__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在t℃时,AgBr在水中的沉淀溶解平衡曲线如下图所示,下列说法不正确的是( )
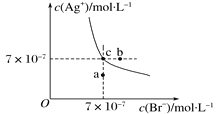
A. 在t℃时,AgBr的Ksp为4.9×10-13
B. 在AgBr饱和溶液中加入NaBr固体,可使溶液由c点变到b点
C. 图中a点对应的是AgBr的不饱和溶液
D. 在t℃时,往AgBr饱和溶液加入KI固体,会产生黄色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的叙述错误的是
A.甲烷和乙烯可以用溴水鉴别
B.煤油是石油的分馏产品,可用于保存少量的钠
C.棉花、蛋白质和油脂都是高分子化合物,水解产物均为电解质
D.用饱和碳酸钠溶液可除去乙酸乙酯中混有的乙酸和乙醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化镁在医药、建筑等行业应用广泛.硫酸镁还原热解制备高纯氧化镁是一种新的探索.以菱镁矿(主要成分为MgCO3 , 含少量FeCO3)为原料制备高纯氧化镁的实验流程如下: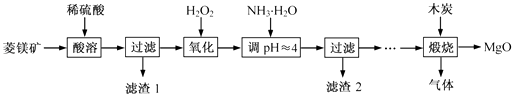
(1)MgCO3与稀硫酸反应的离子方程式为 .
(2)加入H2O2 氧化时,发生反应的化学方程式为 .
(3)滤渣2 的成分是(填化学式).
(4)煅烧过程存在以下反应:2MgSO4+C ![]() 2MgO+2SO2↑+CO2↑
2MgO+2SO2↑+CO2↑
MgSO4+C ![]() MgO+SO2↑+CO↑
MgO+SO2↑+CO↑
MgSO4+3C ![]() MgO+S↑+3CO↑
MgO+S↑+3CO↑
利用如图装置对煅烧产生的气体进行分步吸收或收集.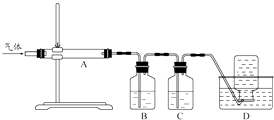
①D中收集的气体可以是(填化学式).
②B中盛放的溶液可以是(填字母).
a.NaOH 溶液 b.Na2CO3 溶液 c.稀硝酸 d.KMnO4溶液
③A中得到的淡黄色固体与热的NaOH溶液反应,产物中元素最高价态为+4,写出该反应的离子方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ,下列热化学方程式正确的是( )
A.CH3OH(l)+ ![]() O2(g)═CO2(g)+2H2O(l);△H=+725.8 kJ/mol
O2(g)═CO2(g)+2H2O(l);△H=+725.8 kJ/mol
B.2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l);△H=﹣1452 kJ/mol
C.2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l);△H=﹣725.8 kJ/mol
D.2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l);△H=+1452 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于弱电解质的说法中正确的是( )
A. 弱电解质需要通电才能发生电离
B. 醋酸溶液达到电离平衡时,不存在CH3COO-+H+![]() CH3COOH
CH3COOH
C. H2SO4是共价化合物,所以它是弱电解质;NaOH是离子化合物,所以它是强电解质
D. 弱电解质溶液中,既有溶质分子,又有溶质电离出来的离子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com