
| 1 |
| 2 |
| 393.5kJ |
| 12 |
| 1 |
| 2 |
| 285.8kJ |
| 2 |
| ||
|
| m |
| M |
| 10.64g |
| 106.4g/mol |
| V |
| Vm |
| 0.896L |
| 22.4L/mol |
| 0.1 |
| 0.04 |
| 0.1 |
| 0.04×2 |
| 1 |
| 0.8 |


 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案科目:高中化学 来源: 题型:
| A、离子键没有方向性和饱和性,共价键有方向性和饱和性 |
| B、配位键在形成时,由成键双方各提供一个电子形成共用电子对 |
| C、金属键的实质是金属中的“自由电子”与金属阳离子形成的一种强烈的相互作用 |
| D、金属键中的“自由电子”为金属阳离子共用 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
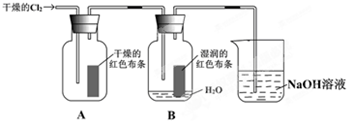
查看答案和解析>>
科目:高中化学 来源: 题型:
2- 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com