
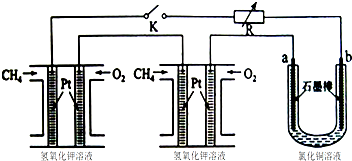
���� ��1���������ȼ�ϵ�������������õ��ӱ���ԭ����������ʧ���ӱ�������
��2��b���ӵ�Դ�ĸ�����ӦΪ����������ͭ��a����������Ϊ��������������������������Ȼ�ͭ��Һ����������ͭ��
��3������b�缫��ͨ�����ĵ缫����������������ͭ���ӷŵ磬����ͭ������$\frac{3.2g}{64g/mol}$=0.05mol��a����������Ϊ�����������������ӷŵ�����������ϵ�ʧ�����غ���㣮
��� �⣺��1���ڼ�����Һ�У�����ȼ�ϵ�ص��ܷ�ӦʽΪCH4+2O2+2OH-=CO32-+3H2O�������ǣ�2O2+4H2O+8e-�T8OH-�������ǣ�CH4-8e-+10OH-�TCO32-+7H2O��
�ʴ�Ϊ��2O2+4H2O+8e-=8OH-��CH4+10OH--8e-=CO32-+7H2O��
��2��b�缫��ͨ�����ĵ缫������������������Ȼ�ͭ��Һ���ܷ�Ӧ����ʽΪ��CuCl2$\frac{\underline{\;���\;}}{\;}$Cu+Cl2�����ʴ�Ϊ��������CuCl2$\frac{\underline{\;���\;}}{\;}$Cu+Cl2����
��3��b�缫��ͨ�����ĵ缫����������������ͭ���ӷŵ磬����ͭ������$\frac{3.2g}{64g/mol}$=0.05mol��a����������Ϊ�����������������ӷŵ��������������ݵ�ʧ�����غ㣬����������ҲΪ0.5mol������v��Cl2��=1.12L��ת�Ƶ�����Ϊ0.05mol��2=0.1mol���ʴ�Ϊ��1.12��0.1��
���� ���⺭�ǵ��غ�ԭ��ص��������ݣ��漰�缫�ж���缫��Ӧʽ��д�����⣬����ʱע���������ԭ�ĽǶ��ж�ԭ��ص��������Լ��缫����ʽ����д���������ѵ���״���Ϊ�缫����ʽ����д��


 ״Ԫ��ȫ��ͻ�Ƶ�����ϵ�д�
״Ԫ��ȫ��ͻ�Ƶ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʵ���� | ʵ��Ŀ�� | T/�� | NO��ʼŨ��mol/L | CO��ʼŨ��mol/L | ͬ�ִ����ıȱ����m2/g |
| �� | Ϊ����ʵ�������� | 280 | 6.50��10-3 | 4.00��10-3 | 80 |
| �� | 6.50��10-3 | 4.00��10-3 | 120 | ||
| �� | ̽���¶ȶԷ�Ӧ���ʵ�Ӱ�� | 360 | 80 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 4�� | B�� | 5�� | C�� | 7�� | D�� | 8�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | A����Է�������С��C��D����Է�������������B����Է������� | |
| B�� | ��AΪ2-�����������ʵ������ͼ������ת�� | |
| C�� | ��A��B��D��Ϊ��״�������CҲһ��Ϊ��״������ | |
| D�� | C��A�ķ�Ӧ����Ϊ�ӳɷ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ijͬѧ��������ʵ�飬̽����ѧ��Ӧ�е������仯��ͨ��ʵ��������Ӧǰ����ձ��е��¶����ߣ����ձ��е��¶Ƚ��ͣ�
ijͬѧ��������ʵ�飬̽����ѧ��Ӧ�е������仯��ͨ��ʵ��������Ӧǰ����ձ��е��¶����ߣ����ձ��е��¶Ƚ��ͣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1mol����ȫ��Ӧ��һ��ʧȥ2NA������ | |
| B�� | 1mol�κ����ʶ�Լ��6.02��1023������ | |
| C�� | �����ʵ�����NO��NO2����Nԭ������Ϊ1mol | |
| D�� | ����£�22.4L����������ԭ������ΪNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��֬������ܶ࣬������ˮ���һ����һ������ͬ | |
| B�� | ���ۡ���ά�ض������࣬����ͨʽ��ͬ�������Dz���Ϊͬ���칹�� | |
| C�� | �ױ��������ڹ����·�Ӧ��Ҫ����2��4-���ȼױ� | |
| D�� | ֻ�����Ƶ�Cu��OH��2����Һ���Լ���������Һ����������Һ�͵�����Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CCl4��PCl3 | B�� | NaCl��HCl | C�� | CO2��SiO2 | D�� | NaH��Na2O2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com