
常温下,下列各组离子在指定溶液中能大量共存的是
A.pH=1的溶液中:Fe2+、NO3-、SO42-、Na+
B.c(H+)/c(OH-)=1012的溶液中:NH4+、Al3+、NO3-、Cl-
C.由水电离的c(H+)=1×10-14mol·L-1的溶液中:Ca2+、K+、Cl-、HCO3-
D.c(Fe3+)=0.1mol·L-1的溶液中:K+、ClO-、SO42-、SCN-
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:高中化学 来源: 题型:
在一定条件下,反应N2+3H22NH3在2 L容器中进行,5 min内NH3的质量增加了1.7 g,则反应速率为( )
A.ν(H2)=0.03 mol·L-1·min-1
B.ν(NH3)=1.7 g·L-1·min-1
C.ν(N2)=0.02 mol·L-1·min-1
D.ν(NH3)=0.01 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
U、V、W、X、Y、Z是原子序数依次增大的六种常见元素,Y的单质在W2中燃烧的产物可使品红溶液褪色。Z的单质在W2中燃烧的产物Z3W4具有磁性。U的单质在W2中燃烧可生成UW和UW2两种气体。X的单质是一种金属,该金属在UW2中剧烈燃烧生成黑、白两种固体。
请回答下列问题:
(1)V的单质分子的结构式为________;XW的电子式为________;U元素在周期表中的位置是________________。
(2)U元素形成的同素异形体的晶体类型可能是(填序号,下同)________,Z单质的晶体类型是________。
①原子晶体 ②离子晶体 ③分子晶体 ④金属晶体
(3)U、V、W形成的10电子氢化物中,U、W的氢化物沸点较低的是(写化学式)________,比较V、W的氢化物的稳定性(写化学式)________________。
(4)YW2气体通入过量的NaOH溶液反应的离子方程式为____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验不能达到实验目的的是( )
①实验窒用无水乙醇和浓硫酸共热到140℃即可制取乙烯
②验证R—X是碘代烷,把R—X与NaOH水溶液混合加热,再往其中加入硝酸银溶液即可
③做醛的还原性实验,向乙醛溶液中加入新制的Cu(OH)2悬浊液即可得到红色沉淀
④检验淀粉已水解,将淀粉与水和稀硫酸加热一段时间后,加入银氨溶液即可
⑤实验室制备乙酸乙酯,把乙醇和乙酸及稀硫酸溶液共热即可
A.①②③④⑤ B.①③④ C.①②③⑤ D.②③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
用1-丁醇、溴化钠和较浓H2SO4混合物为原料,在实验室制备1-溴丁烷,并检验反应的部分副产物。(已知:NaCl+H2SO4(浓)=NaHSO4+HCl↑)现设计如下装置,其中夹持仪器、加热仪器及冷却水管没有画出。请回答下列问题:
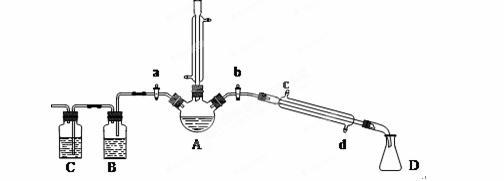
(1)仪器A的名称是 。
(2)关闭a和b、接通竖直冷凝管的冷凝水,给A加热30分钟,制备1-溴丁烷。写出该反应的化学方程式 。
(3)理论上,上述反应的生成物还可能有:丁醚、1-丁烯、溴化氢等。熄灭A处酒精灯,在竖直冷凝管上方塞上塞子,打开a,利用余热继续反应直至冷却,通过B、C装置检验部分副产物。B、C中应盛放的试剂分别是 、 。
(4)在实验过程中,发现A中液体由无色逐渐变成黑色,该黑色物质与浓硫酸反应的化学方程式为 ,可在竖直冷凝管的上端连接一个内装吸收剂碱石灰的干燥管,以免污染空气。
(5)相关有机物的数据如下:
| 物质 | 熔点/0C | 沸点/0C |
| 1-丁醇 | -89.5 | 117.3 |
| 1-溴丁烷 | -112.4 | 101.6 |
| 丁醚 | -95.3 | 142.4 |
| 1-丁烯 | -185.3 | -6.5 |
为了进一步精制1-溴丁烷,继续进行了如下实验:待烧瓶冷却后,拔去竖直的冷凝管,塞上带温度计的橡皮塞,关闭a,打开b,接通冷凝管的冷凝水,使冷水从 (填c或d)处流入,迅速升高温度至 ℃,收集所得馏分。
(6)若实验中所取1-丁醇、NaBr分别为7.4 g、13.0 g,蒸出的粗产物经洗涤、干燥后再次蒸馏得到9.6 g 1-溴丁烷,则1-溴丁烷的产率是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下表各组物质之间通过一步反应能实现如图所示转化关系,且与表中的条件也匹配的是
| 选项 | X | Y | Z | 箭头上为反应条件 |
|
| A | NO | NO2 | HNO3 | ②加H2O | |
| B | Al | NaAlO2 | AlCl3 | ③电解 | |
| C | Fe | FeCl2 | FeCl3 | ①通入少量Cl2 | |
| D | NaOH | NaHCO3 | NaCl | ④依次通入CO2、NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下,将气体X和气体Y各0.16mol充入 10L恒容密闭容器中,发生反应X(g) + Y(g) 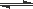 2Z(g) △H < 0,一段时间后达到平衡。反应过程中测定的数据如下表:
2Z(g) △H < 0,一段时间后达到平衡。反应过程中测定的数据如下表:
| t /min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
下列说法正确的是
A.反应前2min的平均速率v(Z) =4.0×10-3mol/(L•min)
B.其他条件不变,降低温度,反应达到新平衡前v(逆) > v(正)
C.该温度下此反应的平衡常数K=1.44
D.其他条件不变,再充入0.2molZ,平衡时X的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
试判断反应:2NaHCO3 (s)= Na2CO3 (s)+ CO2 (g)+ H2O (g)
(1)298K标态下反应的自发方向;(2)反应方向逆转的温度条件。
已知298K时下列热力学数据:
| NaHCO3 (s) | Na2CO3 (s) | CO2 (g) | H2O (g) | |
| △f G | -852 | -1048 | -394.36 | -228.59 |
| △f H | -948 | -1130.8 | -393.51 | -241.82 |
| S | 102 | 135 | 214 | 189 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com