
【题目】[化学——选修5:有机化学基础]甲苯是有机化工的一种重要原料,用它制取利尿“呋塞米”和重要的化工中间体“甲基丙烯酸苄基酯”的合成路线如下(部分步骤和条件省略):
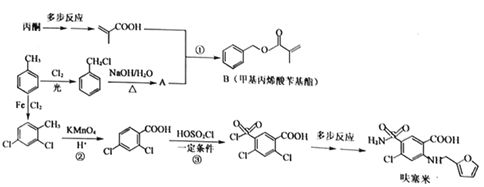
回答下列问题:
(1)A的名称为_________。
(2)反应类型:反应②_________;反应③_________。
(3)反应①的化学方程式_________。
(4)符合下列条件的B的同分异构体(不考虑立体异构)共有_________种。
①某环上只有两个取代基,且每个取代基上碳原子数不超过3个。
②与B具有相同的官能团,1mol该有机物完全水解需要消耗2molNaOH。
写出其中核磁共振氢谱只有5组峰的有机物的结构简式_________。
(5)下列说法正确的是_________。
A.呋塞米既可与强酸反应,又可与强碱反应
B.甲基丙烯酸是丙酸的同系物
C.1mol甲基丙烯酸和丙烯的混合物在氧气中完全燃烧共需要氧气4.5mol
D.可用溴水鉴甲苯和甲基丙烯酸苄基酯
(6)结合以下信息:
① ②RCN
②RCN![]() RCOOH
RCOOH
写出用丙酮和HCN为原料制备化合物![]() 的合成路线__________(其它试剂任选)。
的合成路线__________(其它试剂任选)。
【答案】 苯甲醇 氧化反应 取代反应 ![]() +H2O 15
+H2O 15 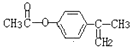 ACD
ACD 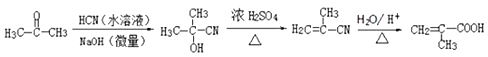 或
或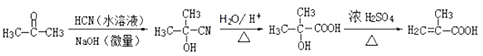
【解析】本题考查有机物的推断和合成,(1)生成A的反应是卤代烃的水解,即A为苯甲醇;(2)反应②利用高锰酸钾的强氧化性,把甲基氧化成羧基,因此此反应为氧化反应;反应③:对比反应前后结构简式,此反应应为取代反应;(3)B为酯,反应①的类型为取代反应或酯化反应,即反应方程式为![]() +H2O ;(4)与B具有相同的官能团,1mol该有机物完全水解需要消耗2molNaOH,以及B的结构简式,符合条件的同分异构体中含有
+H2O ;(4)与B具有相同的官能团,1mol该有机物完全水解需要消耗2molNaOH,以及B的结构简式,符合条件的同分异构体中含有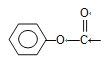 ,符合条件的是
,符合条件的是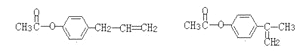 、
、![]() 、
、![]() ,两个取代基位置应为邻间对三种,因此符合条件的同分异构体有5×3=15,核磁共振氢谱有5种峰,说明有5种不同的氢原子,符合条件的是
,两个取代基位置应为邻间对三种,因此符合条件的同分异构体有5×3=15,核磁共振氢谱有5种峰,说明有5种不同的氢原子,符合条件的是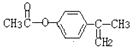 ;(5)A、呋塞米的结构简式中含有羧基和氨基,羧基能与强碱反应,氨基显碱性,能与强酸反应,故A正确;B、甲基丙烯酸中含有碳碳双键,丙酸中不含碳碳双键,因此两者不互为同系物,故B错误;C、有机物燃烧的通式为CxHyOz+(x+y/4-y/2)O2→xCO2+y/2H2O,1mol甲基丙烯酸燃烧消耗氧气物质的量为(4+6/4-2/2)mol=4.5mol,1mol丙烯燃烧消耗氧气物质的量为(3+6/4)mol=4.5mol,故C正确;D、甲苯不能使溴水褪色,甲基丙烯酸苄基酯中含有碳碳双键,能使溴水褪色,故D正确;(6)根据题目中所给信息,丙酮先于HCN在NaOH溶液中发生反应,生成(CH3)2C(OH)CN,然后在酸中水解成(CH3)2C(OH)COOH,最后发生消去反应,得到目标产物,其合成路线为:
;(5)A、呋塞米的结构简式中含有羧基和氨基,羧基能与强碱反应,氨基显碱性,能与强酸反应,故A正确;B、甲基丙烯酸中含有碳碳双键,丙酸中不含碳碳双键,因此两者不互为同系物,故B错误;C、有机物燃烧的通式为CxHyOz+(x+y/4-y/2)O2→xCO2+y/2H2O,1mol甲基丙烯酸燃烧消耗氧气物质的量为(4+6/4-2/2)mol=4.5mol,1mol丙烯燃烧消耗氧气物质的量为(3+6/4)mol=4.5mol,故C正确;D、甲苯不能使溴水褪色,甲基丙烯酸苄基酯中含有碳碳双键,能使溴水褪色,故D正确;(6)根据题目中所给信息,丙酮先于HCN在NaOH溶液中发生反应,生成(CH3)2C(OH)CN,然后在酸中水解成(CH3)2C(OH)COOH,最后发生消去反应,得到目标产物,其合成路线为: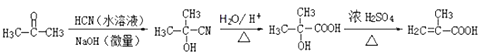 或
或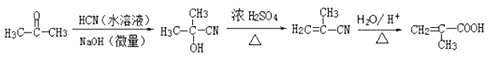 。
。


 高中必刷题系列答案
高中必刷题系列答案科目:高中化学 来源: 题型:
【题目】如图是四种常见有机物分子的比例模型示意图。下列说法正确的是( )
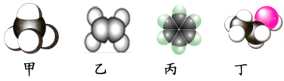
A. 甲是甲烷,甲烷能使酸性KMnO4溶液褪色
B. 乙是乙烯,乙烯可与溴水发生取代反应使溴水褪色
C. 丙是苯,苯在空气中燃烧时产生带有浓烟的火焰
D. 丁是乙酸,一定条件下乙酸能跟乙醇发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过去五年,环保部向水污染、大气污染宣战,生态环境保护取得明显成效。
Ⅰ.污水中硝酸盐浓度过高,会诱发一些水体产生亚硝胺类的致癌物质。
(1)在缺氧条件下,脱氮菌(反硝化菌)以甲醇作碳源,将NO3-还原成N2的过程如下:
反硝化作用过程:NO3-![]() NO2-
NO2-![]() NO
NO![]() N2O
N2O![]() N2
N2
阶段①会生成CO2,请写出此反应的离子方程式:__________________;阶段③生成的N2O是一种强温室气体,但却可用作火箭燃料的氧化剂,,其优点是___________________。
(2)Murphy等人通过调节溶液pH为10.25,利用铝粉将NO3-转变成N2,实现化学脱氮。
要转化0.01molNO3-,需_________gAl。
Ⅱ.CO2和CH4均为温室气体,如何减少它们的排放、充分利用能源是当今社会的重要课题。
(3)二氧化碳经催化氢化可转化成绿色能源乙醇。已知:
①2H2(g)+O2(g)=2H2O(g)△H= -483.6 kJ·mol-1
②CH3CH2OH(l)+3O2(g)=2CO2(g)+3H2O(l) △H=-1366.8kJ·mol-1
③H2O(l)=H2O(g)△H=+44.0kJ·mol-1
则二氧化碳与氢气转化成乙醇和液态水的热化学方程式为:_________。
(4)CO2和CH4在催化剂作用下可转化为合成气(CO和H2):CO2(g)+CH4(g)![]() 2CO(g)+2H2(g) △H=+247.3kJ·mol-1。向容积为1L的密闭容器中通入反应物和生成物共5.25mol,在T℃时发生反应,气体体积分数及化学反应速率与反应时间的关系如下图所示:
2CO(g)+2H2(g) △H=+247.3kJ·mol-1。向容积为1L的密闭容器中通入反应物和生成物共5.25mol,在T℃时发生反应,气体体积分数及化学反应速率与反应时间的关系如下图所示:
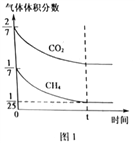
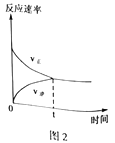
①T℃时,反应的平衡常数K=______。向平衡体系中再加入CO2、CH4、H2和CO各0.5mol,平衡将_________移动(填“向左”、“向右”或“不”)。
②写出一种既能加快化学反应速率又能提高CH4转化率的措施______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己二酸是一种重要的化工原料和合成中间体。已知:室温下,己二酸微溶于水,当温度由28℃升至78℃时,其溶解度可增大20倍。某实验小组利用绿色氧化剂H2O2氧化环己烯合成己二酸,反应和制备装置如下:
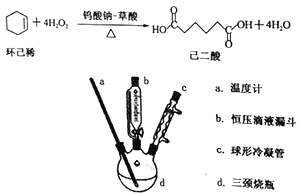
主要实验步骤:
①在100mL三颈烧瓶中依次加入1.50g钨酸钠0.57g草酸和34mL30%过氧化氢溶液,室温下磁力搅拌20min。
②用恒压滴液漏斗缓慢加入8.0mL的环己烯,继续搅拌并加热回流2小时,停止加热。
③将反应液迅速转入烧杯中,冷却至室温后再用冰水浴冷却,有大量晶体析出。抽滤,并用少量冰水洗涤,即可得到己二酸晶体粗品。
回答下列问题:
(1)本实验中使用带刻度的恒压滴液漏斗的主要作用有_________、_________。
(2)步骤③中用冰水洗涤晶体的目的是______________________________________。
己二酸晶体粗品可利用_________方法进一步获得纯品。
(3)取0.1480g己二酸(Mr=146.0)样品置于250mL锥形瓶中,加入50mL蒸馏水溶解,再加入2滴指示剂,用0.1000mol/Ld的NaOH标准溶液滴定至终点,消耗NaOH溶液的体积为20.00mL。
①本实验应选择_________(填“甲基橙”“石蕊”或“酚酞”)溶液作指示剂。
②判断滴定终点的方法是_________________________。
③样品中己二酸的质量分数为_________%(保留4位有效数字)。
(4)实验小组通过改变环己烯的用量来探究物料比对产率的影响,实验结果如下图所示。
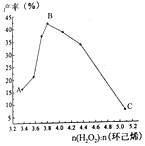
结合图像分析产率变化的可能原因:
①A点→B点:___________________________________________;
②B点→C点:____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】当人误食重金属盐类时,可以喝大量牛奶、蛋清或豆浆解毒。重金属盐使人中毒的原因是___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在三个体积均为 1.0L的恒容密闭容器中发生反应:2CH3OH(g) CH3OCH3(g) + H2O(g) 下列说法正确的是( )
容器 编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |
CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
I | 387 | 0.20 | 0.080 | 0.080 |
II | 387 | 0.40 | ||
III | 207 | 0.20 | 0.090 | 0.090 |
A. 该反应的正反应为吸热反应
B. 达到平衡时,容器I中的CH3OH体积分数比容器II中的小
C. 容器I中反应到达平衡所需时间比容器III的长
D. 若起始时向容器I中充入0.15mol 的CH3OH、0.15mol 的CH3OCH3和0.10mol 的H2O,则反应将向正反应方向进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以石油化工的一种产品A(乙烯)为主要原料合成一种具有果香味的物质E的生产流程如下:
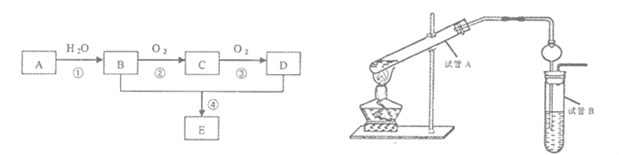
(1)写出步骤①的化学方程式_______________反应类型__________;
步骤②的化学方程式______________反应类型__________;
(2)某同学欲用上图装置制备物质E,回答以下问题:
①试管A发生反应的化学方程式_______________________;
②试管B中的试剂是______________________;分离出乙酸乙酯的实验操作是______________(填操作名称),用到的主要玻璃仪器为____________________;
③插入右边试管的导管接有一个球状物,其作用为_______________________。
(3)为了制备重要的有机原料——氯乙烷(CH3—CH2Cl),下面是两位同学设计的方案。
甲同学:选乙烷和适量氯气在光照条件下制备,原理是:
CH3—CH3+Cl2 ![]() CH3—CH2Cl+HCl
CH3—CH2Cl+HCl
乙同学:选乙烯和适量氯化氢在一定条件下制备,原理是:
CH2=CH2+HCl→CH3—CH2Cl
你认为上述两位同学的方案中,合理的是____,简述你的理由:____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com