
 某课外小组的同学拟用废铝箔制取硫酸铝晶体,已知铝的物种类别与溶液pH关系如图所示,实验中可选用的试剂:处理过的铝箔;2.0mol•L-1NaOH溶液:2.0mol•L-1硫酸
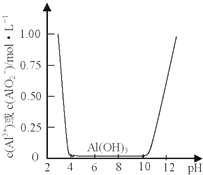
某课外小组的同学拟用废铝箔制取硫酸铝晶体,已知铝的物种类别与溶液pH关系如图所示,实验中可选用的试剂:处理过的铝箔;2.0mol•L-1NaOH溶液:2.0mol•L-1硫酸分析 铝与氢氧化钠反应生成偏铝酸钠与氢气,过滤,向滤液中加入硫酸,由图可知,调节pH在4~10时生成氢氧化铝沉淀,再过滤、洗涤,向沉淀中加入稀硫酸,至恰好溶解,从溶液中获得晶体,需要蒸发浓缩、冷却结晶,再进行过滤、洗涤、干燥得到硫酸铝晶体.
解答 解:铝与氢氧化钠反应生成偏铝酸钠与氢气,过滤,向滤液中加入硫酸,由图可知,调节pH在4-10时生成氢氧化铝沉淀,再过滤、洗涤,向沉淀中加入稀硫酸,至恰好溶解,从溶液中获得晶体,需要蒸发浓缩、冷却结晶,再进行过滤、洗涤、干燥得到硫酸铝晶体.
③根据图片知,pH在4~10时生成氢氧化铝沉淀,所以该步骤是:向滤液中滴加2.0mol•L-1硫酸,不断搅拌,调节溶液pH为4~10,从而得到氢氧化铝沉淀,
故答案为:滤液中滴加2.0mol•L-1硫酸,不断搅拌,调节溶液pH为4~10;
⑤该实验目的是制取硫酸铝晶体,所以用得到的氢氧化铝沉淀制取硫酸铝溶液,其操作方法是:沉淀中不断加入2.0mol•L-1硫酸至恰好溶解,
故答案为:沉淀中不断加入2.0mol•L-1硫酸至恰好溶解;
⑥从溶液中获得晶体采用加热浓缩、冷却结晶的方法,所以该操作为蒸发浓缩,
故答案为:蒸发浓缩.
点评 本题考查制备实验方案设计,侧重考查学生制备、操作等基本能力,明确实验原理是解本题关键,难度中等,回答时注意明确硫酸的浓度.


科目:高中化学 来源: 题型:选择题
| A. | 2H++2e-═H2↑ | B. | Fe-2e-═Fe2+ | ||
| C. | 2H2O+O2+4e-═4OH- | D. | Fe-3e-═Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 原子序数依次增大的A、B、C、D、E五种短周期元素,A是原子半径最小的元素,B的单质分子中有三对共用电子,C最外层电子数是次外层电子数的3倍,A、D同主族,E原子电子数比C原子电子数多5个,请回答下列问题:
原子序数依次增大的A、B、C、D、E五种短周期元素,A是原子半径最小的元素,B的单质分子中有三对共用电子,C最外层电子数是次外层电子数的3倍,A、D同主族,E原子电子数比C原子电子数多5个,请回答下列问题: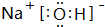 ,以W溶液作为电解质溶液,E棒与铁棒分别作为电极构成原电池,则负极的电极反应式Al-3e-+4OH-=AlO2-+2H2O;
,以W溶液作为电解质溶液,E棒与铁棒分别作为电极构成原电池,则负极的电极反应式Al-3e-+4OH-=AlO2-+2H2O;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蚕丝、羊毛和淀粉分别属于纤维素、蛋白质和多糖 | |
| B. | 石油裂解和油脂皂化都是高分子生成小分子的过程 | |
| C. | 分子式为C2H4O2且能与NaOH溶液反应的有机物一定是乙酸 | |
| D. | 乙醇、乙酸和乙醛能用新制Cu(OH)2悬浊液鉴别 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al箔插入稀HNO3中无现象因Al箔表面被HNO3氧化,形成致密的氧化膜 | |
| B. | “硝基苯制备”实验中,将温度计插入水浴,但水银球不能与烧杯底部和烧杯壁接触 | |
| C. | “中和滴定”实验中,容量瓶和锥形瓶用蒸馏水洗净后即可使用,滴定管用蒸馏水洗净后,必须干燥或润洗后方可使用 | |
| D. | 除去干燥CO2中混有的少量SO2,可将混合气体依次通过盛有酸性KMnO4溶液、浓硫酸的洗气瓶 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
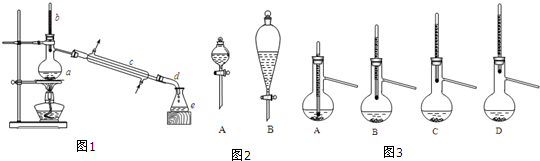
| 正丁醇 | 冰醋酸 | 乙酸正丁酯 | 正丁醚 | |
| 密度/(g/cm3) | 0.810 | 1.049 | 0.882 | 0.7689 |
| 沸点/℃ | 118.0 | 118.1 | 126.1 | 142 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 鉴别对象 | 所用试剂 | 实验现象 |
| 苯和苯酚 | 加入FeCl3溶液 | 苯无现象,苯酚溶液呈紫色 |
| 苯和甲苯 | 加入酸性高锰酸钾溶液 | 苯不能使高锰酸钾溶液褪色,甲苯能使高锰酸钾溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碘和氯化钾 | B. | 金刚石和冰晶石 | C. | 二氧化硅和干冰 | D. | 冰和冰醋酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;物质⑤的结构式O=C=O.
;物质⑤的结构式O=C=O.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com