
【题目】有一含NaCl、Na2CO3·10H2O和NaHCO3的混合物,某同学设计如图所示的实验装置,通过测量反应产生的CO2和H2O的质量,来确定该混合物中各组分的质量分数。
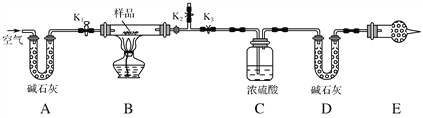
(1)实验步骤:
①按图(夹持仪器未画出)组装好实验装置后,首先进行的操作是_________。
②称取样品,并将其放入硬质玻璃管中;称量装浓硫酸的洗气瓶C的质量和装碱石灰的U形管D的质量。
③打开活塞K1、K2,关闭K3,缓缓鼓入空气数分钟,其目的是________________。
④关闭活塞K1、K2,打开K3,点燃酒精灯加热至不再产生气体。装置B中发生反应的化学方程式为_________________________________________。
⑤打开活塞K1,缓缓鼓入空气数分钟,然后拆下装置,再次称量洗气瓶C的质量和U形管D的质量。
(2)关于该实验方案,请回答下列问题。
①若加热反应后不鼓入空气,对测定结果的影响是___________________。
②E处干燥管中盛放的药品是________,其作用是__________________ ________________,如果实验中没有该装置,则会导致测量结果NaHCO3的质量________(填“偏大”、“偏小”或“无影响”)。
③若样品质量为w g,反应后C、D装置增加的质量分别为m1 g、m2 g,则混合物中Na2CO3·10H2O的质量分数为________(用含w、m1、m2的代数式表示)。
【答案】 检查装置气密性 除去装置中的水蒸气和二氧化碳 2NaHCO3![]() Na2CO3+H2O↑+CO2↑ Na2CO3·10H2O
Na2CO3+H2O↑+CO2↑ Na2CO3·10H2O![]() Na2CO3+10H2O↑ Na2CO3·10H2O和NaHCO3的质量分数测定结果偏小,NaCl的质量分数测定结果偏大 碱石灰 防止空气中的CO2和水蒸气进入D中影响测定结果 偏大
Na2CO3+10H2O↑ Na2CO3·10H2O和NaHCO3的质量分数测定结果偏小,NaCl的质量分数测定结果偏大 碱石灰 防止空气中的CO2和水蒸气进入D中影响测定结果 偏大 ![]() ×100%
×100%
【解析】(1)①由实验原理可知,实验需要通过测量D装置内碱石灰的增重,计算生成的二氧化碳的质量,通过测量C装置装置,计算生成的水的质量,故应首先检验装置的气密性;
③装置内有空气,含有水蒸气和二氧化碳,影响水蒸气和二氧化碳质量的测定,打开活塞K1、K2,关闭活塞K3,实验前要通入空气,赶走装置中含有水蒸气和二氧化碳,减少误差;
④含NaCl、Na2CO310H2O和NaHCO3的混合物加热时,碳酸氢钠分解生成碳酸钠、二氧化碳和水,碳酸钠晶体失去结晶水生成碳酸钠,反应的化学方程式为:2NaHCO3![]() Na2CO3+H2O↑+CO2↑;Na2CO310H2O
Na2CO3+H2O↑+CO2↑;Na2CO310H2O![]() Na2CO3+10H2O↑;
Na2CO3+10H2O↑;
(2)①若加热反应后不鼓入空气,生成水蒸气质量和二氧化碳质量测定结果会减小,碳酸氢钠依据二氧化碳计算,而Na2CO310H2O的测定是根据生成水的总质量计算的,则测得Na2CO310H2O的含量将偏小对测定结果的影响是NaCl偏大,NaHCO3 偏小,Na2CO310H2O偏小;
②干燥管中盛放的是碱石灰,碱石灰能吸收空气中的水蒸气和二氧化碳,所以干燥管的作用是防止空气中的CO2和水蒸气进入影响测定结果,若撤去E装置,则测定的碳酸氢钠的质量偏大;
③D装置中增加的质量为二氧化碳的质量,碳酸氢钠分解生成的水蒸气的质量为x.
2NaHCO3![]() Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
18g 44g
xm2g
x=![]() g,
g,
装置C吸收的是水蒸气,包括碳酸氢钠分解生成的和十水碳酸钠分解生成的,十水碳酸钠分解生成的水蒸气的质量=m1g-![]() g=
g=![]() g.
g.
设十水碳酸钠的质量为y.
Na2CO310H2O![]() Na2CO3+10H2O
Na2CO3+10H2O
286g 180g


科目:高中化学 来源: 题型:
【题目】若把元素周期表原先的主、副族号取消,由左到右按原顺序编为18列。如碱金属为第1列,稀有气体为第18列,按这个规定,下列说法中不正确的是 ( )
A. 计算机芯片的组成元素Si位于第14列
B. 第10列元素全部是金属元素
C. 第3列元素元素的种类最多
D. 只有第2列元素的原子最外层有2个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活密切相关。下列有关叙述正确的是
A. “一带一路”被誉为现代丝绸之路,丝绸属于纤维素
B. 电解水制氢气可缓解能源危机,实现节能环保
C. “雨后彩虹”是一种与胶体有关的自然现象
D. 烧制“明如镜、声如磬”的瓷器时未涉及化学变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列涉及有机物的性质或应用的说法不正确的是 ( )
A. 淀粉、纤维素、蛋白质都是天然高分子化合物
B. 用于奥运“祥云”火炬的丙烷是一种清洁燃料
C. 用大米酿的酒在一定条件下密封保存,时间越长越香醇
D. 纤维素、蔗糖、葡萄糖和脂肪在一定条件下都可发生水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素性质呈周期性变化的决定因素是 ( )
A. 元素相对原子质量依次递增 B. 元素的最高正化合价呈周期性变化
C. 元素原子最外层电子排布呈周期性变化 D. 元素金属性或非金属性呈周期性变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在理论上不能用于设计原电池的化学反应是
A.H2SO4(aq)+BaCl2(aq)===2HCl(aq)+BaSO4(s) ΔH<0
B.2CH3OH(l)+3O2(g)===2CO2(g)+4H2O(l) ΔH<0
C.4Fe(OH)2(s)+2H2O(l)+O2(g)===4Fe(OH)3(s) ΔH<0
D.3Cu(s)+8HNO3(aq)===3Cu(NO3)2(aq)+2NO(g)+4H2O(l) ΔH<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是
A.电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-===Cl2↑
B.氢氧燃料电池的负极反应式:O2+2H2O+4e-===4OH-
C.粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu-2e-===Cu2+
D.钢铁发生电化学腐蚀的负极反应式:Fe-3e-===Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列文字表述与反应的离子方程式对应且正确的是()
A. SO2通入NaClO溶液中:SO2+2ClO-+H2O![]() SO32-+2HC1O
SO32-+2HC1O
B. Fe3O4与足量稀HNO3反应:3Fe3O4+28H++NO3-=9Fe3++NO2↑+14H2O
C. NaHSO4溶液与 Ba(OH)2溶液混合后显中性:Ba2++OH-+H++SO42-=BaSO4↓+H2O
D. NaNO2溶液中加入酸性KMnO4溶液:2MnO4-+5NO2-+6H+=2Mn2++5NO3-+3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ca(ClO)2与浓盐酸反应会生成Cl2 , 该反应的化学方程式为:
Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O
(1)浓盐酸在反应中显示出来的性质是 (填写字母).
A.只有还原性
B.还原性和酸性
C.只有氧化性
D.氧化性和酸性
(2)产生0.3mol Cl2 , 则转移的电子的物质的量为 mol.
(3)此反应的离子反应方程式为 .
(4)用双线桥法表示该氧化还原反应中电子转移的方向和数目 .
(5)配平方程式: KMnO4+HCl(浓)═ KCl+MnCl2+Cl2↑+H2O.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com