
在平衡体系2NO+O2  2NO2中通入18O组成的氧气,重新达到平衡后,则18O
2NO2中通入18O组成的氧气,重新达到平衡后,则18O
A.只存在于O2中
B.只存在于NO2中
C.只存在于O2和NO2中
D.存在于NO、O2、NO2
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案科目:高中化学 来源: 题型:
下列各组离子因发生氧化还原反应而不能大量共存的是( )
A.Fe3+、OH-、SO 、CO
、CO
B.Cu2+、Fe2+、H+、NO
C.Ag+、Na+、SO 、Cl-
、Cl-
D.K+、H+、CO 、MnO
、MnO
查看答案和解析>>
科目:高中化学 来源: 题型:
有关下列能量转化的认识不正确的是( )。
A.植物的光合作用使得太阳能转化为了化学能
B.人类使用照明设备是将电能转化为了光能
C.生物体内的化学变化过程在能量转化上比在体外发生的一些能量转化更为合理、有效
D.燃料燃烧时只是将化学能转化为了热能
查看答案和解析>>
科目:高中化学 来源: 题型:
我国“蛟龙”号载人潜水器已成功下潜至海中7020米处。“蛟龙”号载人潜水器的外壳是耐超高压的钛合金,下面有关说法中正确的是
A.钛合金是一种新型金属单质 B.钛合金硬度比成分金属大
C.钛合金的性质与钛单质相同 D.青铜、合金钢和硬铝都是合金
查看答案和解析>>
科目:高中化学 来源: 题型:
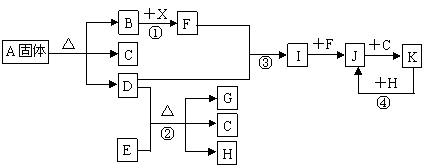 下图表示各物质之间的转化关系。已知:常温下B、D、F、G、I、J是气体, F、G是空气中的主要成分,D是一种碱性气体。A中阴、阳离子个数比是1∶1, E是一种黑色氧化物,H是紫红色金属单质。(部分生成物和反应条件省略)
下图表示各物质之间的转化关系。已知:常温下B、D、F、G、I、J是气体, F、G是空气中的主要成分,D是一种碱性气体。A中阴、阳离子个数比是1∶1, E是一种黑色氧化物,H是紫红色金属单质。(部分生成物和反应条件省略)
请按要求填空:
(1)A物质的化学式是 ▲ ;
(2)反应③的化学方程式是 ▲ ;
反应④的离子方程式是 ▲ ;
(3)反应①中产生标准状况下1.12L气体F,则转移的电子数目是 ▲ ;
(4)检验溶液A中阳离子的方法是 ▲
;
(5)反应②中氧化剂是 ▲ ;
查看答案和解析>>
科目:高中化学 来源: 题型:
对于Zn(s)+H2SO4(aq)===ZnSO4(aq)+H2(g) ΔH=?的化学反应,下列叙述不正确的是
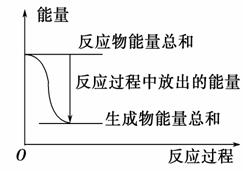
A.反应过程中能量关系如上图表示,则该反应为放热反应
B.若将其设计为原电池,当有32.5 g锌溶解时,正极放出气体一定为11.2 L
C.化学反应的焓变与反应方程式的计量系数有关
D.若将该反应设计成原电池,锌为负极
查看答案和解析>>
科目:高中化学 来源: 题型:
向某密闭容器中加入0.3 mol A、0.1 mol C和一定量的B三种气体。一定条件下发生反应,各物质的浓度随时间变化如甲图所示[t0~t1阶段的c(B)变化未画出]。乙图为t2时刻后改变条件平衡体系中正、逆反应速率随时间变化的情况,且四个阶段都各改变一种反应条件且互不相同,t3~t4阶段为使用催化剂。下列说法中正确的是
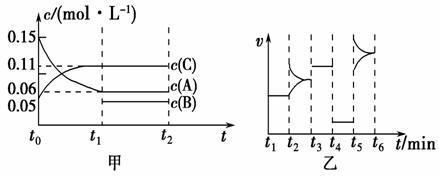
A.若t1=15 s,用A的浓度变化表示t0~t1阶段的平均反应速率为0.004 mol·L-1·s-1
B.该容器的容积为2 L,B的起始物质的量为0.02 mol
C.t4~t5阶段改变的条件一定为减小压强
D.t5~t6阶段,容器内A的物质的量减少了0.06 mol,而此过程中容器与外界的热交换总量为a kJ,该反应的热化学方程式:3A(g) B(g)+2C(g) ΔH=-50a kJ·mol-1
B(g)+2C(g) ΔH=-50a kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH=-57.3 kJ/mol,则下列说法中正确的是
A.浓硫酸和稀NaOH溶液反应,生成 l mol水时放热57.3 kJ
B.含l molH2SO4的稀硫酸与足量稀NaOH溶液中和后,放热为57.3 kJ
C.1L 0.l mol/L CH3COOH与1L 0.l1 mol/L NaOH溶液反应后放热为5.73 kJ
D.1L 0.l mol/L HNO3与1L 0.l1 mol/L NaOH溶液反应后放热为5.73 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
冰晶胞中水分子的空间排列方式与金刚石晶胞类似,如下图:
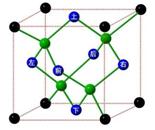
(1)一个水分子含_____个孤电子对,水分子能与很多金属离子形成配合物,请写出它与铜离子形成的一种蓝色的配合物离子的化学式为__________。
(2)每个冰晶胞平均占有____个水分子,冰的熔点远低于金刚石熔点的原因是_____________________。
(3)实验测得冰中氢键的作用力为18.5 kJ/mol,而冰的熔化热为5.0 kJ/mol,这说明冰熔化成水,氢键_____________(填全部或部分)被破坏。
(4)假如冰晶胞边长为a cm,则冰的密度是________________g·cm-3
(阿伏伽德罗常数用NA表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com