
 看如图完成下面的填空,写出电极反应式和总反应式.
看如图完成下面的填空,写出电极反应式和总反应式.分析 Cu、Fe和稀硫酸构成原电池中,Fe失电子发生氧化反应作负极,电极反应为Fe-2e-=Fe2+,Cu为正极,正极上氢离子得电子发生还原反应,电极反应为2H++2e-=H2,总反应为Fe+2H+=Fe2++H2↑.
解答 解:(1)Cu、Fe和稀硫酸构成原电池中,Fe失电子发生氧化反应作负极,电极反应为Fe-2e-=Fe2+,
故答案为:负;Fe-2e-=Fe2+;氧化;
(2)Cu、Fe和稀硫酸构成原电池中,Fe失电子作负极,Cu为正极,正极上氢离子得电子发生还原反应,则其正极的电极反应为:2H++2e-=H2↑;
故答案为:正;2H++2e-=H2↑;还原;
(3)根据反应原理知,电池总反应为Fe+2H+=Fe2++H2↑,
故答案为:Fe+2H+=Fe2++H2↑.
点评 本题考查了原电池原理,掌握电极的判读和电极方程式书写,侧重于基本原理应用的考查,题目难度不大,注意基础知识的积累.


 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案科目:高中化学 来源: 题型:推断题
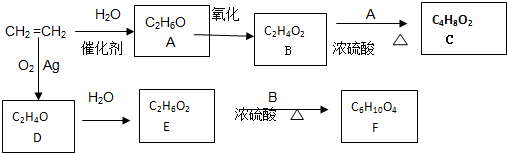
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
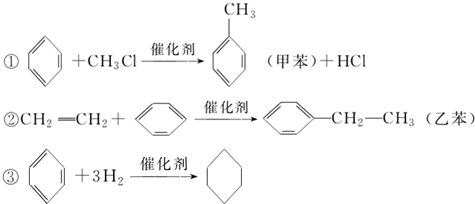
| A. | 反应①、②、③加成反应 | |
| B. | 溴水中加入苯,二者可发生取代反应 | |
| C. | 乙苯中所有碳原子一定在同一平面上 | |
| D. | 能用溴水判断反应②所得的乙苯中是否混有乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| 元素编号 | 元素特征信息 |
| A | 其单质是密度最小的物质 |
| B | 阴离子带两个单位负电荷,单质是空气的主要成分之一 |
| C | 其阳离子与B的阴离子有相同的电子层结构,且与B可以形成两种离子化合物 |
| D | 其氢氧化物和氧化物都有两性,与C同周期 |
| E | 与C同周期,原子半径在该周期最小 |
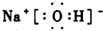 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 手机上用的锂离子电池属于二次电池 | |
| B. | 充电电池可以无限制地反复使用 | |
| C. | 甲醇燃料电池可把化学能转化为电能 | |
| D. | 废旧电池不能乱扔,需回收处理 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Fe3+、SO42- | B. | CO32-、Cl-、SO42- | C. | Ca2+、Br-、SO42- | D. | Na+、SO42-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com