
【题目】元素①~⑦在周期表中的相对位置如图所示。

请回答下列问题。
(1)⑤的元素符号是____________,其最高正化合价是____________。
(2)①~⑦中金属性最强的是____________(填元素符号),能证明⑥比②的非金属性强的事实是____。
(3)③④形成的化合物是____________或____________。
(4)④⑥⑦原子半径由大到小的顺序是__________________(用元素符号表示);④的最高价氧化物对应的水化物是____________,它与⑥的最高价氧化物对应的水化物反应的离子方程式是__________________。
【答案】![]()
![]()
![]()
![]() 为强酸、
为强酸、![]() 为弱酸(其他合理答案也可)
为弱酸(其他合理答案也可) ![]()
![]()
![]() NaOH
NaOH 
【解析】
由元素在周期表中的位置,可知①为![]() 、②为
、②为![]() 、③为
、③为![]() 、④为
、④为![]() 、⑤为
、⑤为![]() 、⑥为
、⑥为![]() 、⑦为
、⑦为![]() ,据此分析。
,据此分析。
由元素在周期表中的位置,可知①为![]() 、②为
、②为![]() 、③为
、③为![]() 、④为
、④为![]() 、⑤为
、⑤为![]() 、⑥为
、⑥为![]() 、⑦为
、⑦为![]() ;
;
(1)⑤的元素符号为![]() ,硅的最外层有4个电子,其最高正化合价为
,硅的最外层有4个电子,其最高正化合价为![]() ;
;
(2)①~⑦中金属性最强的是![]() 元素;⑥为
元素;⑥为![]() 、②为
、②为![]() ,由于
,由于![]() 为强酸、
为强酸、![]() 为弱酸,则
为弱酸,则![]() 的非金属性比
的非金属性比![]() 强;
强;
(3)③④分别为![]() 、
、![]() 元素,二者形成的化合物为
元素,二者形成的化合物为![]() 、
、![]() ;
;
(4)![]() 、
、![]() 和
和![]() 位于同一周期,从左到右原子半径逐渐减小,则原子半径大小为
位于同一周期,从左到右原子半径逐渐减小,则原子半径大小为![]() ;④为
;④为![]() ,其最高价氧化物对应的水化物是
,其最高价氧化物对应的水化物是![]() ;⑥的最高价氧化物对应的水化物为
;⑥的最高价氧化物对应的水化物为![]() ,硫酸与氢氧化钠反应生成硫酸钠和水,反应的离子方程式为
,硫酸与氢氧化钠反应生成硫酸钠和水,反应的离子方程式为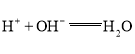 。
。


科目:高中化学 来源: 题型:
【题目】下列各组性质比较中,正确的是()
①沸点:![]()
②离子还原性:![]()
③酸性:![]()
④金属性:![]()
⑤气态氢化物稳定性:![]()
⑥半径:![]()
A.①②③B.③④⑤⑥C.②③④D.①③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方案中,能达到相应实验目的的是
A | B | C | D | |
方案 |
|
|
|
|
目的 | 分离甲烷和氯气发生反应后得到的液态混合物 | 验证石蜡油分解的产物是乙烯 | 检验乙烯、乙炔混合气中的乙烯 | 制备并检验乙炔的性质 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是中学化学中常见物质之间的一些反应关系,其中部分产物未写出。常温下X是固体,B和G是液体,其余均为气体。根据下图关系推断:
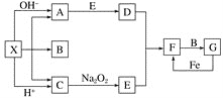
(1)写出化学式:X_______,A________,B_______。
(2)实验室收集气体D和F的方法依次是_______法、________法。
(3)写出C→E的化学方程式:____________。
(4)请写出A与E反应生成D的化学方程式:_______________
(5)检验物质A的方法和现象是________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知![]() 、
、![]() 是第三周期的两种金属元素,且
是第三周期的两种金属元素,且![]() 的原子半径比
的原子半径比![]() 的原子半径大,则下列叙述正确的是( )
的原子半径大,则下列叙述正确的是( )
A.![]() 的原子序数比
的原子序数比![]() 的原子序数小
的原子序数小
B.![]() 的离子比
的离子比![]() 的离子得电子能力强
的离子得电子能力强
C.![]() 的失电子能力比
的失电子能力比![]() 的失电子能力强
的失电子能力强
D.![]() 的离子半径比
的离子半径比![]() 的离子半径小
的离子半径小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲是短周期元素中原子半径最小的元素,乙的气态氢化物的水溶液显碱性,丙是短周期元素中原子半径最大的元素,丁是地壳中含量最多的金属元素。
(1)写出四种元素的名称:甲______,乙______,丙______,丁______。
(2)乙、丙、丁三种元素的原子半径从大到小的顺序是________(填元素符号,下同)![]() ________
________![]() ________。
________。
(3)写出乙、丙、丁的最高价氧化物对应的水化物相互反应的化学方程式:__________________、__________________、__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废旧光盘金属层中含有金属Ag(其他金属微量忽略不计),从光盘中提取金属Ag的工艺流程如下。请回答下列问题:

(1)“氧化”阶段需在80℃条件下进行,使用的加热方式为_________。
(2)NaClO溶液与Ag反应的产物为AgCl、NaOH和O2,该反应的化学方程式为________。有人提出用HNO3代替NaClO氧化Ag,从反应产物的角度分析,其缺点是_________。
(3)“过滤Ⅰ”中洗涤难溶物的实验操作为__________。
(4)常用10%的氨水溶解AgCl固体,AgCl与NH3·H2O按1∶2反应可生成Cl-和一种阳离子______(填离子符号)的溶液。实际反应中,即使氨水过量,“废渣”中也含有少量AgCl固体,可能的原因是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种气态烷烃和一种气态烯烃,它们分子里的碳原子数相等.将1.0体积这种混合气体在氧气中完全燃烧,生成2.0体积的CO2和2.4体积的水蒸气(气体体积均在相同状况下测定),则混合气体中烷烃和烯烃的体积比为( )
A.3:1 B.1:3 C.2:3 D.3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮及其化合物与人类生产、生活息息相关。回答下列问题:
(1)氮的氢化物之一肼(N2H4)是一种油状液体,常做火箭燃料,与水任意比互溶,并且沸点高达113℃。在肼分子中N原子的杂化方式是___,肼易溶于水的原因是___,肼的沸点高达113℃的原因是___。
(2)N2F2是氮的氟化物之一,lmol N2F2中含有___mol ![]() 键;N和F中电负性较大的是____。
键;N和F中电负性较大的是____。
(3)氮与钠形成的化合物有Na3N和NaN3。
①Na3N能与水剧烈反应生成NaOH和NH3,则Na3N属于___晶体。
②NaN3用于汽车的安全气囊中,当发生车祸时迅速分解放出氮气,使安全气囊充气。反应原理为2NaN3+CuO![]() Na2O+2Cu+3N2↑。写出两种与
Na2O+2Cu+3N2↑。写出两种与![]() 互为等电子体的分子或离子:___(填化学式)。
互为等电子体的分子或离子:___(填化学式)。
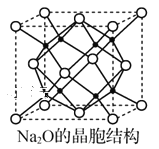
(4)Na2O的晶胞结构如图所示,晶胞边长为566pm,晶胞中氧原子的配位数为___,Na2O晶体的密度为___g·cm3(只要求列算式,不必计算出结果) 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com