
| A. | 1:1 | B. | 1:2 | C. | 5:7 | D. | 7:5 |
分析 把铝粉和某铁氧化物xFeO•yFe2O3粉末配成铝热剂,分成两等份,一份在高温下恰好完全反应生成铁与氧化铝,Fe与盐酸反应生成FeCl2与H2,另一份直接加入足量的NaOH溶液分反应生成偏铝酸钠与氢气,前后两种情况下生成的气体质量比是5:7,设氢气物质的量分别为5mol、7mol,根据电子转移守恒计算n(Fe)、n(Al),再根据Fe元素总物质的量及电子转移守恒列方程计算x、y的值.
解答 解:把铝粉和某铁氧化物xFeO•yFe2O3粉末配成铝热剂,分成两等份,一份在高温下恰好完全反应生成铁与氧化铝,Fe与盐酸反应生成FeCl2与H2,令一份直接加入足量的NaOH溶液分反应生成偏铝酸钠与氢气,前后两种情况下生成的气体质量比是5:6,设氢气物质的量分别为5mol、6mol,
根据电子转移守恒,n(Fe)=n(H2)=5mol,n(Al)=$\frac{7mol×2}{3}$=$\frac{14}{3}$mol,
假设x molFeO、ymol Fe2O3,
由Fe元素守恒可知:x+2y=5,由电子转移守恒,可得:2x+2y×3=$\frac{14}{3}$×3解得x=1,y=2,
故x:y=1:2,
故选B.
点评 本题考查混合物的计算,难度中等,清楚反应过程是关键,注意混合物的计算中守恒的运用,注意运用赋值法简化计算.


科目:高中化学 来源: 题型:选择题
| A. | 用稀HNO3溶解Fe3O4固体的离子方程式:Fe3O4+8H+═2Fe3++Fe2++4H2O | |
| B. | 将SO2通入H2S溶液中的化学方程式:SO2+2H2S═3S+2H2O | |
| C. | 氢溴酸与氢氧化钠发生中和反应的离子方程式:H++OH-═H2O | |
| D. | 向明矾溶液中加入过量的氨水发生反应的离子方程式:Al3++4OH-═${AlO}_{2}^{-}$+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学式 | 电离常数(25℃) |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
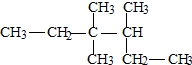
| A. | 3,4,4-三甲基己烷 | B. | 3,3-二甲基-2-乙基戊烷 | ||
| C. | 3,3,4-三甲基己烷 | D. | 3,3-二甲基-4-乙基戊烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
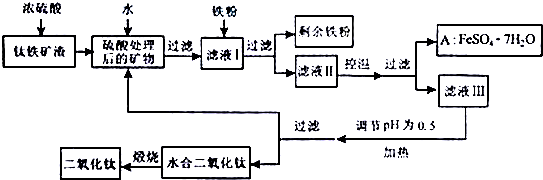
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
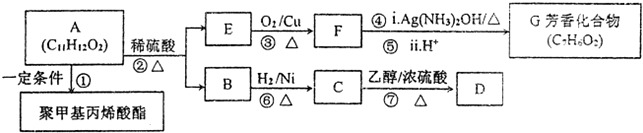
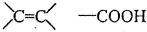 ;检验其宫能团所用化学试剂有溴的四氯化碳(或酸性高锰酸钾溶液)、碳酸氢钠溶液(或石蕊试剂).
;检验其宫能团所用化学试剂有溴的四氯化碳(或酸性高锰酸钾溶液)、碳酸氢钠溶液(或石蕊试剂). .
. (CH3)2CHCOOCH2CH3+H2O.
(CH3)2CHCOOCH2CH3+H2O.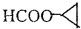 .
.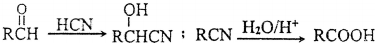
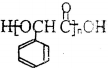 ,方框内写中间体的结构简式,在“→”上方或下方写反应所需条件或试剂.
,方框内写中间体的结构简式,在“→”上方或下方写反应所需条件或试剂.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸、纯碱、漂白粉 | B. | 硫酸、烧碱、小苏打 | ||
| C. | 硫酸氢钠、生石灰、醋酸钠 | D. | 磷酸、熟石灰、苛性钠 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com