
【题目】某树脂的单体是丙烯酸钠(CH2=CHCOONa),关于丙烯酸钠的说法不正确的是
A.存在顺反异构
B.经加聚反应得树脂
C.水溶液呈碱性
D.使酸性KMnO4溶液褪色
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列物质的除杂方案正确的是
选项 | 被提纯的物质 | 杂质 | 除杂试剂 | 除杂方法 |
A | CO2(g) | SO2(g) | 饱和Na2CO3溶液、浓H2SO4 | 洗气 |
B | NH4Cl(ap) | Fe3+(ap) | NaOH溶液 | 过滤 |
C | NaCl(s) | KNO3(g) | AgNO3溶液 | 过滤 |
D | Cu(s) | Ag(s) | CuSO4 | 电解法 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2004年美国圣路易斯大学研制了一种新型的乙醇电池,它用磺酸类质子溶剂,在200oC左右时供电,乙醇电池比甲醇电池效率高出32倍且更安全。电池总反应为:C2H5OH +3O2 ==2CO2 +3H2O,电池示意如图,下列说法不正确的是
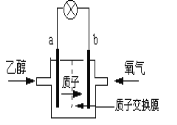
A.a极为电池的负极
B.电池工作时电流由b极沿导线经灯泡再到a极
C.电池工作时,1mol乙醇被还原时就有6mol电子转移
D.电池正极的电极反应为:4H+ + O2 + 4e— =2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用饱和氯化铁溶液制取氢氧化铁胶体,正确的操作是
A.将FeCl3溶液滴入蒸馏水中即可
B.将FeCl3溶液滴入热水中,生成棕黄色液体即可
C.将FeCl3溶液滴入沸水中,并继续煮沸至生成红褐色沉淀即可
D.将FeCl3溶液滴入沸水中,并继续煮沸至生成红褐色液体即可
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某研究小组采用电解法处理石油炼制过程中产生的大量H2S废气的工艺流程。该方法对H2S的吸收率达99%以上,并可制取H2和S。下列说法正确的是
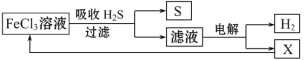
A.吸收H2S的离子方程式为:Fe3++H2S====Fe2++S↓+2H+
B.电解过程中的阳极反应主要为:2Cl--2e-====Cl2↑
C.该工艺流程体现绿色化学思想
D.实验室可用点燃充分燃烧的方法消除H2S污染
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2气体是一种常用的消毒剂,我国从2000年起逐步用ClO2代替氯气对饮用水进行消毒。
(1)消毒水时,ClO2还可将水中的Fe2+、Mn2+等转化成Fe(OH)3和MnO2等难溶物除去,在这个过程中,Fe2+、Mn2+的化合价升高,说明ClO2具有 性。
(2)工业上可以通过下列方法制取ClO2,请完成该反应化学方程式:
2KClO3+ SO2 = 2ClO2 + 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,物质A~E转化关系如图所示,其中A为单质,常温下E为无色液体。
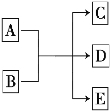
(1)若A、C、D均含氯元素,C为氯碱工业的原料,D溶液具有漂白性,则A与B反应的化学方程式_____________________;D溶液可使淀粉KI溶液显蓝色,则D与KI在溶液中反应的离子方程式是 ;检验C中所含阴离子的实验方法是_____________________。
(2)若A为红色金属,B为某酸的浓溶液,D为可形成酸雨的无色气体。A与B反应的化学方程式是_______________。amol A与足量的B充分反应后,将产生的D通入NaOH溶液中,恰好完全反应,则所需NaOH的物质的量的范围是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】应对雾霾污染、改善空气质量需要从多方面入手。
I.研究发现,NOx是雾霾的主要成分之一,NOx主要来源于汽车尾气。
已知:N2(g)+O2(g)![]() 2NO(g) △H=+180.50kJ·mol-1
2NO(g) △H=+180.50kJ·mol-1
2CO(g)+O2(g)![]() 2CO2(g) △H=-566.00 kJ·mol-1
2CO2(g) △H=-566.00 kJ·mol-1
为了减轻大气污染,人们提出在汽车尾气排气管口采用催化剂将NO和CO转化成无污染气体参与大气循环,写出该反应的热化学方程式 。
II.开发利用清洁能源可减少污染,解决雾霾问题。甲醇是一种可再生的清洁能源,具有广阔的开发和应用前景,一定条件下用CO和H2合成CH3OH:CO(g)+2H2(g)![]() CH3OH(g),在2L密闭容器中充入物质的量之比为1:2的CO和H2,在催化剂作用下充分反应。平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如下图所示。
CH3OH(g),在2L密闭容器中充入物质的量之比为1:2的CO和H2,在催化剂作用下充分反应。平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如下图所示。

(1)该反应的反应热△H 0(填“>”或“<”),压强的相对大小与P1 P2(填“>”或“<”)。
(2)该反应化学平衡常数表达式为 。
(3)下列各项中,不能说明该反应已经达到平衡的是 。
A.容器内气体压强不再变化
B.v(CO):v(H2):v(CH3OH)=1:2:1
C.容器内的密度不再变化
D.容器内混合气体的平均相对分子质量不再变化
E.容器内各组分的质量分数不再变化
(4)某温度下,在保证H2浓度不变的情况下,增大容器的体积,平衡 (填字母)。
A.向正反应方向移动 B.向逆反应方向移动 C.不移动
作出此判断的依据是 。
III.依据燃烧反应原理,合成的甲醇可以设计如图所示的燃料电池装置。

(1)负极电极反应式为 。
(2)电池工作时,若电流强度为I,1个电子所带电量为q,NA为阿伏伽德罗常数的值,则该装置每分钟消耗甲醇的物质的量为 mol(假设化学能全部转化为电能)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com