
 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | 通常蔗糖和淀粉都不显还原性 | |
| B. | 纤维素分子是由葡萄糖单元组成的,可以表现出一些多元醇的性质 | |
| C. | 油脂是热能最高的营养物质 | |
| D. | 铜盐可以使蛋白质产生盐析 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 纯净的苯酚是粉红色的晶体 | |
| B. | 有特殊的气味 | |
| C. | 易溶于乙醇、乙醚等有机溶剂,不易溶于冷水 | |
| D. | 苯酚有毒,沾在皮肤上,可用浓NaOH溶液洗涤 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
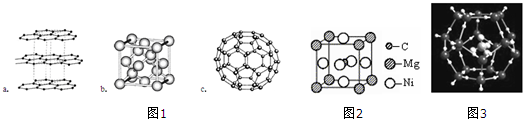
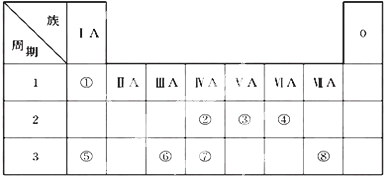
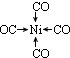 ;写出基态Ni原子的电子排布式1s22s22p63s23p63d84s2.
;写出基态Ni原子的电子排布式1s22s22p63s23p63d84s2.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 铜是负极,铜片上有气泡产生 | |
| B. | 铜片是正极,该电极周围溶液pH不变 | |
| C. | 电子流从锌片经导线流向铜片 | |
| D. | 氢离子在锌片表面被还原 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 配制银氨溶液:向氨水中加入过量的硝酸银溶液 | |
| B. | 银镜反应:向银氨溶液中滴加葡萄糖溶液后,热水浴 | |
| C. | 检验蔗糖的水解产物:先加碱中和,再滴入新制的氢氧化铜中加热 | |
| D. | 淀粉水解:向淀粉溶液中加入唾液,加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 12 | B. | 16 | C. | 20 | D. | 25 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
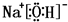 或
或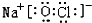 .
.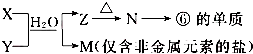
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com