
分析 混合溶液中c(CH3COO-)=c(Na+),根据电荷守恒得c(OH-)=c(H+),据此确定溶液酸碱性,醋酸钠溶液呈碱性,要使混合溶液呈中性,醋酸的物质的量应该稍微大于氢氧化钠,据此分析.
解答 解:由于混合溶液中c(CH3COO-)=c(Na+),根据电荷守恒可得c(OH-)=c(H+),即溶液呈中性.而若醋酸和氢氧化钠恰好完全反应,所得的醋酸钠溶液呈碱性,故要使混合溶液呈中性,醋酸的物质的量应该稍微大于氢氧化钠,而醋酸和氢氧化钠浓度相等,所以醋酸体积大于氢氧化钠,故答案为:>;
点评 本题考查了弱电解质的电离及盐类水解,结合电荷守恒和盐类的水解规律来分析,难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
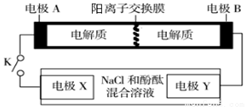 某二次电池充、放电的化学方程式为:2K2S2+KI3$?_{充电}^{放电}$ K2S4+3KI.与其它设备连接的电路如图所示.当闭合开关K时,X附近溶液先变红.则下列说法正确的是( )
某二次电池充、放电的化学方程式为:2K2S2+KI3$?_{充电}^{放电}$ K2S4+3KI.与其它设备连接的电路如图所示.当闭合开关K时,X附近溶液先变红.则下列说法正确的是( )| A. | 放电时,电极A发生还原反应 | |
| B. | A的电极反应式为:3I--2e-=I3- | |
| C. | 当有0.1 mol K+通过离子交换膜,X电极上产生气体1.12 L(标准状况下 | |
| D. | 电池充电时,B电极要与外电源的正极相连,电极上发生还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
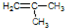 .
. .该分子的所有碳原子能否在一个平面上(填“能”或“不能”)不能.
.该分子的所有碳原子能否在一个平面上(填“能”或“不能”)不能.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al2O3熔点高,可用作耐高温材料 | B. | SiO2能与HF反应,可用作光导纤维 | ||
| C. | KAl(SO4)2易溶于水,可用作净水剂 | D. | Fe2O3能与酸反应,可用作红色涂料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3 kJ•mol-1(燃烧热) | |
| B. | OH-(aq)+H+(aq)=H2O(l)△H=+57.3 kJ•mol-1(中和热) | |
| C. | 2H2(g)+O2(g)=2H2O(g)△H=-483.6 kJ•mol-1(反应热) | |
| D. | 2NO2=O2+2NO△H=+116.2 kJ•mol-1(反应热) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 电离能/kJ•mol-1 | I1 | I2 | I3 | I4 |
| A | 578 | 1 817 | 2 745 | 11 578 |
| B | 738 | 1 451 | 7 733 | 10 540 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com