
| A. | 无色溶液中加入AgNO3溶液得白色沉淀,加稀盐酸不消失,可能存在Cl-或SO42- | |
| B. | 无色溶液中滴加BaCl2溶液得白色沉淀,加稀硝酸不溶解,则一定含有SO42- | |
| C. | 用CCl4萃取碘水中的碘,下层呈紫红色 | |
| D. | 加入盐酸,生成的气体能使澄清石灰水变浑浊,则原溶液中一定有大量CO32- |
分析 A、氯化银、硫酸钡是白色的不溶于硝酸的沉淀;
B、无色溶液中滴加BaCl2溶液得白色沉淀,加稀硝酸不溶解,沉淀可以是氯化银还可以是硫酸钡;
C、用CCl4萃取碘水中的碘,碘单质在四氯化碳中的溶解度更大;
D、能和盐酸反应产生二氧化碳气体的可以是碳酸根还可以是碳酸氢根离子等.
解答 解:A、无色溶液中加入AgNO3溶液得白色沉淀,加稀盐酸不消失,可能存在Cl-或SO42-、SO32-,故A错误;
B、无色溶液中滴加BaCl2溶液得白色沉淀,加稀硝酸不溶解,则含有硫酸根离子或是银离子中的至少一种,故B错误;
C、用CCl4萃取碘水中的碘,碘单质在四氯化碳中的溶解度更大,四氯化碳和水互不相溶,密度大于水,所以下层呈紫红色,故C正确;
D、加入盐酸,生成的气体能使澄清石灰水变浑浊,则原溶液中有大量碳酸根离子、碳酸氢根离子等离子中的至少一种,故D错误.
故选C.
点评 本题考查了常见离子的检验方法,题目难度中等,注意掌握常见离子的性质及检验方法,明确离子检验时,必须排除干扰离子,确保检验方案的严密性.


 金钥匙试卷系列答案
金钥匙试卷系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
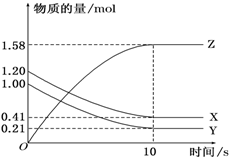 一定温度下,某1L体积固定的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,请回答下列问题:
一定温度下,某1L体积固定的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 乙醇 | 溴乙烷 | 1-丁醇 | 1-溴丁烷 | |
| 密度/g•cm-3 | 0.7893 | 1.4604 | 0.8098 | 1.2758 |
| 沸点/℃ | 78.5 | 38.4 | 117.2 | 101.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
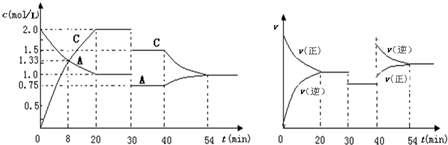
| A. | 0~20min用A物质表示反应的平均速率为0.005mol•L-1•min-1 | |
| B. | 该反应的正反应为吸热反应 | |
| C. | x=1,且30min时改变的反应条件是减压 | |
| D. | 在25min、35min、55min时化学平衡常数分别为K1、K2、K3,则K3>K2>K1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com