
����Ŀ������[KAl(SO4)2��12H2O]���������������й㷺��;������ˮ�ľ�������ֽ��ҵ����ʩ������ʳƷ��ҵ�ķ��ͼ��ȡ������������ķ�����������(��Al��Al2O3������SiO2��FeO��xFe2O3)���Ʊ������������������£��ش��������⣺
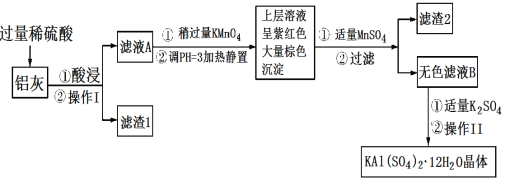
��1��������ˮ��ԭ����______________(�����ӷ���ʽ��ʾ)��
��2����������________��������������Ũ����__________�����ˡ�ϴ�ӡ����
��3��������ҺA���Ƿ����Fe2�����Լ���__________(ֻ��һ���Լ�)��
��4��������Ͷ������������Һ����������Ļ�ѧ����ʽ��__________������ҺA�м��������ط�����Ӧ�����ӷ���ʽΪ(��������MnO4-ת��ΪMn2��)��_______��
��5����֪����pH��3�����������£�MnO4-����Mn2����Ӧ����MnO2������MnSO4������Ӧ�����ӷ���ʽΪ��________������2���е�������________��
���𰸡�Al3����3H2O![]() Al(OH)3(����)��3H�� ���� ��ȴ�ᾧ ���Ը��������Һ(�����軯����Һ) 2Al��2NaOH��2H2O=2NaAlO2��3H2�� 5Fe2����MnO4-��8H��=5Fe3����Mn2����4H2O 3Mn2����2MnO4-��2H2O=5MnO2����4H�� MnO2��Fe(OH)3
Al(OH)3(����)��3H�� ���� ��ȴ�ᾧ ���Ը��������Һ(�����軯����Һ) 2Al��2NaOH��2H2O=2NaAlO2��3H2�� 5Fe2����MnO4-��8H��=5Fe3����Mn2����4H2O 3Mn2����2MnO4-��2H2O=5MnO2����4H�� MnO2��Fe(OH)3
��������
��1��������ǿ�������Σ�![]() ˮ����������������壬�ܹ�����ˮ�������������γɳ�������ȥ���Ӷ��ﵽ��ˮ��Ŀ�ġ��䷴Ӧԭ���÷���ʽ��ʾ��Al3����3H2O
ˮ����������������壬�ܹ�����ˮ�������������γɳ�������ȥ���Ӷ��ﵽ��ˮ��Ŀ�ġ��䷴Ӧԭ���÷���ʽ��ʾ��Al3����3H2O![]() Al(OH)3(����)��3H����
Al(OH)3(����)��3H����
��2���������ǽ������Թ�������Һ����IJ������й��ˡ�������������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ�����͵õ�������
�ʴ𰸣����ˣ���ȴ�ᾧ��
��3��������ҺA���Ƿ����![]() �ķ����������軯����Һ���������ɫ������֤������
�ķ����������軯����Һ���������ɫ������֤������![]() ���ʴ𰸣����軯����Һ��
���ʴ𰸣����軯����Һ��
��4��2Al��2NaOH��2H2O=2NaAlO2��3H2����Al2O3+2OH-=2AlO2-+H2O������ҺA�м��������ص�Ŀ����ʹ![]() ת��Ϊ
ת��Ϊ![]() ��������Ӧ�����ӷ���ʽΪ5Fe2����MnO4-��8H��=5Fe3����Mn2����4H2O��
��������Ӧ�����ӷ���ʽΪ5Fe2����MnO4-��8H��=5Fe3����Mn2����4H2O��
��5�����ݱ������ݿ�֪����Һ��pH=3ʱ![]() �����γɳ���
�����γɳ���![]() ��������ɵ÷���ʽ3Mn2����2MnO4-��2H2O=5MnO2����4H����������Һ��pH=3�����������ijɷֺ���MnO2��Fe(OH)3��
��������ɵ÷���ʽ3Mn2����2MnO4-��2H2O=5MnO2����4H����������Һ��pH=3�����������ijɷֺ���MnO2��Fe(OH)3��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ����Cl2��FeCl2��KSCN�����Һ�ķ�Ӧ����ʵ��̽����
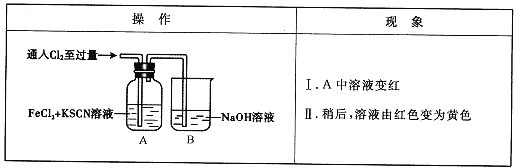
��1��B�з�Ӧ�����ӷ���ʽ��____��
��2��A����Һ����ԭ����____��
��3��Ϊ��̽������II��ԭ��ͬѧ��������ʵ�顣
��ȡA�л�ɫ��Һ���Թ��У�����NaOH��Һ���к��ɫ�������ɣ�����Һ��һ������_____��
��ȡA�л�ɫ��Һ���Թ��У����������KSCN��Һ�����յõ���ɫ��Һ��
��ͬѧ��ʵ��֤��������������ԭ����SCN����Cl2�����˷�Ӧ��
��4����ͬѧ����SCN�����ܱ�Cl2�����ˣ����ֽ����������о���
������ʾ��SCN���ĵ���ʽΪ![]()
����ͬѧ��ΪSCN����̼Ԫ��û�б�������������_________��
��ȡA�л�ɫ��Һ���Թ��У������������ữ��BaCl2��Һ��������ɫ�������ɴ�֤��SCN���б�������Ԫ����__________��
��ͨ��ʵ��֤����SCN���е�Ԫ��ת��ΪNO3-������ʵ�鷽����____��
����SCN����Cl2��Ӧ����1 mol CO2����ת�Ƶ��ӵ����ʵ�����______mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�����Ļ���������ܱ������з�����Ӧ��mA��g��+nB��g��![]() pC��g�����ﵽƽ��ʱ��ά���¶Ȳ��䣬�����������С��ԭ����1/2�����ﵽ�µ�ƽ��ʱ������C��Ũ�ȱ�Ϊԭƽ��ʱ��1.9����������˵����ȷ���ǣ� ��
pC��g�����ﵽƽ��ʱ��ά���¶Ȳ��䣬�����������С��ԭ����1/2�����ﵽ�µ�ƽ��ʱ������C��Ũ�ȱ�Ϊԭƽ��ʱ��1.9����������˵����ȷ���ǣ� ��
A. m+n��pB. m+n��p
C. ƽ��������Ӧ�����ƶ�D. C��������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CO2����Դ����������Ч����CO2�ŷţ��������̼��Դ��
��1��CO2��CH4�����������Ƶúϳ�����CH4(g)��CO2(g)![]() 2CO(g)��2H2(g)
2CO(g)��2H2(g)
��֪��C(s)+2H2(g)=CH4(g) ��H=��75 kJ��mol1
C(s)+O2(g)=CO2(g) ��H=��394 kJ��mol1
C(s)+![]() O2(g)===CO(g) ��H=��111 kJ��mol1
O2(g)===CO(g) ��H=��111 kJ��mol1
�ٸô�������Ӧ����H=____ kJ��mol1�����������CH4ƽ��ת���ʵ�������____�����ţ���
A�����µ�ѹ B�����¸�ѹ C�����¸�ѹ D�����µ�ѹ
��ij�¶��£������Ϊ2 L�������м���2 mol CH4��1 mol CO2�Լ���������������Ӧ���ﵽƽ��ʱCO2��ת������50%����ƽ�ⳣ��Ϊ______mol2��L2�����п��жϸ÷�Ӧ�ﵽƽ�����_________�����ţ���
A����λʱ��������n mol��CH4��ͬʱ����n mol��H2 B��v(CH4):v(CO)=1:2
C�������л��������ܶȲ��ٷ����仯 D�������е�ѹǿ���ֲ���
��2��CO2���Ա�(NH4)2CO3��Һ����ӦΪ(NH4)2CO3(aq)��H2O(l)��CO2(g)=2NH4HCO3(aq)����H��Ϊ�о��¶ȶ�(NH4)2CO3����CO2Ч�ʵ�Ӱ�죬��ij�¶�T1�£���һ������(NH4)2CO3��Һ�����ܱ������У�������һ������CO2����(�õ�����Ϊϡ�ͼ�)����tʱ�̣����������CO2�����Ũ�ȡ�Ȼ��ֱ����¶�ΪT2��T3��T4��T5�£�����������ʼʵ���������䣬�ظ�����ʵ�飬������ͬʱ����CO2����Ũ�ȣ����ϵ��ͼ1������H______(�>������������<��)0��
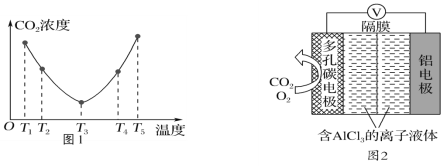
��3��O2������Al-CO2��ع���ԭ����ͼ2��ʾ���õ�ص�����������Ч����CO2����ط�Ӧ����Al2(C2O4)3����Ҫ�Ļ���ԭ�ϡ�
��صĸ�����Ӧʽ��________________________________��
��ص�������Ӧʽ��6O2��6e��=6O��6CO2��6O=3C2O42-��6O2
��Ӧ������O2��������_________________��
��4��CO2���Ա�NaOH��Һ������������Һc(HCO3-)��c(CO32-) �� 2��1����ҺpH��________��(�����£�H2CO3��K1��4��10��7��K2��5��10��11)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڷ�Ӧ11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4�У���֪Cu3P��PΪ-3�ۣ���15molCuSO4��������P�����ʵ���Ϊ
A. 1.5mol B. 5.5mol C. 3mol D. 2.5mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ʵ�����������ķ�Ӧ��Zn+2HCl= ZnCl2+H2��������13.0gZn����һ����2mol/Lϡ�����ַ�Ӧ��һ��ʱ���Zn����ʣ��.
(1)��˫���Ż����ű������ת�Ƶķ������Ŀ
(2)�Ƚ�H+��Zn2+������ǿ��
(3)������������������������
(4)����ZnCl2�����ʵ���Ϊ���٣�
(5)��״���£�������ռ������������壿
(6)��Ӧ��ת�Ƶĵ��ӵĸ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ȲΪ��Ҫԭ�Ͽ��Ժϳɾ�����ϩ���۱�ϩ����ȶ�����ͼ��ʾ���йغϳ�·��ͼ��
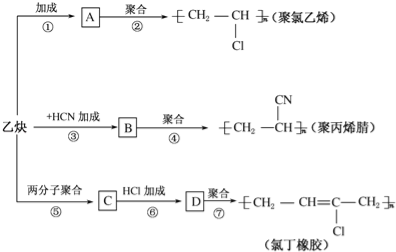
��֪��Ӧ��nCH2�TCH��CH�TCH2![]()
![]()
��������и��⣺
��1��д�����ʵĽṹ��ʽ��A ��C ��
��2��д����Ӧ�Ļ�ѧ����ʽ
��Ӧ���� ��
��Ӧ���� ��
��Ӧ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������NaCl��Na2SO4��NaNO3�Ļ���ѡ���ʵ����Լ���ȥ���ʣ��Ӷ��õ�������NaNO3���壬��Ӧ��ʵ��������ͼ��ʾ��
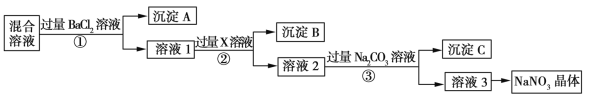
��ش��������⣺
��1��д��ʵ���������������ʵĻ�ѧʽ���Լ�X__������A___��
��2������ʵ�������Т٢ڢ۲���Ҫ���е�ʵ�������__����������ƣ���
��3������ʵ�������м������Na2CO3��Һ��Ŀ����__________��
��4������ʵ�鷽���õ�����Һ3�п϶�����____���ѧʽ�����ʡ�Ϊ�˽��������⣬��������Һ3�м���������__���ѧʽ����
��5���ڢٲ����������֤���ӵ�BaCl2��Һ�ѹ�����________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ն�����ж��ص������������ϵ�������Ƭ֮һ���Ȼ��崼��Ӱ��������������֮һ���ṹ��ͼ��ʾ������˵����ȷ����
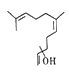
A. �����ʵĻ�ѧʽ��C15H26O
B. �����ʲ���ʹ���Ը��������Һ��ɫ
C. �����ʵ�ͬ���칹������Ƿ����廯����
D. �����ʿ��Է����ӳɷ�Ӧ�����ܷ�����ȥ��Ӧ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com