
| A、用碱式滴定管量取0.10 mol?L-1的Na2CO3溶液22.10 mL |
| B、配制一定浓度的氢氧化钠溶液时,将氢氧化钠固体放在纸片上称量 |
| C、用广范pH试纸测某HCl溶液pH=3.6 |
| D、用玻璃棒蘸取HCl溶液滴到湿润的pH试纸上,测其pH |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、在10-15mL之间 |
| B、恰好在15mL处 |
| C、小于15mL |
| D、大于15mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
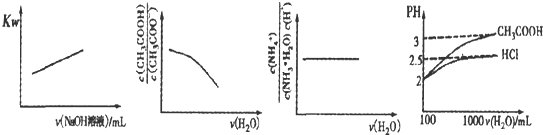
| A、图甲表示在纯水中加人0.0lmol.L-1NaOH溶液,Kw与NaOH溶液体积变化关系 | ||
B、图乙表示将1 mol?L-1 CH3COONa溶液加水稀释,溶液中
| ||
C、图丙表示0.1mol?L-1NH3?H2O加水稀释,溶液中
| ||
| D、图丁表示100 mLpH=2的HCl和CH3COOH加水稀释到1000 mL时pH变化与水的体积的变化关系 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原电池中阳离子向负极移动 |
| B、用铝质铆钉接铁板,铁易被腐蚀 |
| C、粗铜精炼时,粗铜接直流电源的正极 |
| D、白铁(镀锌)的表面一旦破损,铁腐蚀加快 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素编号 | 元素性质或原子结构 |
| T | M层上有2对成对电子 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
查看答案和解析>>
科目:高中化学 来源: 题型:
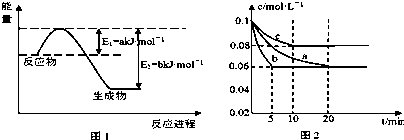
| T/(K) | 298 | 398 | 498 | … |
| K | 4.1×106 | K1 | K2 | … |
查看答案和解析>>
科目:高中化学 来源: 题型:
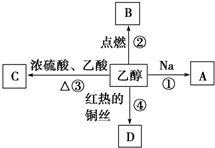 乙醇是生活中常见的有机物,能进行如图所示的多种反应,A、B、C、D都是含碳化合物.写出下列反应的化学方程式及对应的反应类型:
乙醇是生活中常见的有机物,能进行如图所示的多种反应,A、B、C、D都是含碳化合物.写出下列反应的化学方程式及对应的反应类型:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com