

 ;该物质溶于水后的溶液呈碱性(填“酸”、“碱”或“中”).
;该物质溶于水后的溶液呈碱性(填“酸”、“碱”或“中”). .
. 分析 由元素在周期表中位置,可知A为氢、B为He、C为Na、D为碳、E为氮、F为氧、G为Si、H为硫、I为Cl,由此分析解答.
解答 解:(1)同周期自左而右金属性减弱,同主族自上而下金属性增强,故上述元素中Na的金属性最强,故答案为:钠;
(2)同周期从左到右半径逐渐减小,所以半径最小的是氯原子,故答案为:Cl;
(3)中心元素非金属性越强对应氢化物越稳定,非金属性S>Si,所以氢化物中较稳定的是H2S,故答案为:H2S;
(4)在一定条件下,A与E可形成一种极易溶于水的气态化合物为NH3,电子式为 ,所以结构式为:
,所以结构式为: ,氨气溶于水后的溶液呈碱性,故答案为:
,氨气溶于水后的溶液呈碱性,故答案为: ;碱;
;碱;
(5)CO2属于共价化合物,用电子式表示形成过程为 ,故答案为:
,故答案为: .
.
点评 本题考查元素周期表与元素周期律应用,比较基础,注意理解掌握用电子式表示物质或化学键的形成.


科目:高中化学 来源: 题型:选择题
| A. | SiO2是氧化剂 | B. | SiO2发生氧化反应 | ||
| C. | C表现出氧化性 | D. | C被还原 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
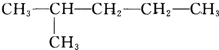 ⑥
⑥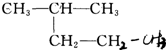
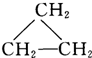
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:rW>rZ>rY | |
| B. | 化合物X2Y、ZY、ZX2中化学键的类型相同 | |
| C. | 由X、Y、Z、W组成的化合物的水溶液可能显酸性 | |
| D. | 由Y元素形成的离子与W元素形成的离子的电子数不可能相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气有毒,不可用于自来水的杀菌消毒 | |
| B. | Al(OH)3受热分解生成H2O并吸收大量的热量,可用作阻燃剂 | |
| C. | 二氧化硅不与强酸反应,可用玻璃容器盛放氢氟酸 | |
| D. | Na2O2具有强氧化性,可用作呼吸面具的供氧剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳在氧气中的燃烧 | B. | 葡萄糖在人体内氧化分解 | ||
| C. | Ba(OH)2•8H2O与NH4Cl反应 | D. | 锌粒与稀H2SO4反应制取H2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com