
| A. | 质子数为78 | B. | 中子数为53 | C. | 质量数为131 | D. | 核外电子数为78 |
分析 元素符号左上角数字表示质量数、左下角数字表示质子数,所以该核素中质子数是53、质量数是131,中子数=质量数-质子数,原子中核外电子数等于质子数,据此分析解答.
解答 解:元素符号左上角数字表示质量数、左下角数字表示质子数,所以该核素中质子数是53、质量数是131,中子数=质量数-质子数=131-53=78,原子中核外电子数等于质子数=53,
A.质子数是53,故A错误;
B.中子数是78,故B错误;
C.质量数是131,故C正确;
D.核外电子数是53,故D错误;
故选C.
点评 本题考查质子数、中子数、质量数、核外电子数之间的关系,明确这几个物理量之间的关系即可解答,知道元素符号周围各个方向上数字的含义,题目难度不大.


科目:高中化学 来源: 题型:选择题
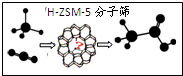 最近我国科研人员发现在温和的反应条件下,甲烷和二氧化碳在锌修饰的
最近我国科研人员发现在温和的反应条件下,甲烷和二氧化碳在锌修饰的| A. | 有机物 | B. | 共价化合物 | C. | 电解质 | D. | 离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
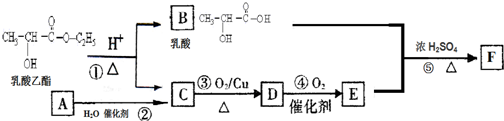
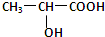 +CH3COOH$→_{△}^{浓硫酸}$
+CH3COOH$→_{△}^{浓硫酸}$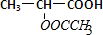 +H2O;
+H2O;查看答案和解析>>
科目:高中化学 来源: 题型:填空题
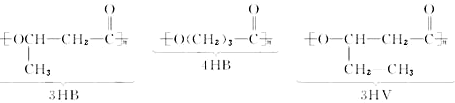
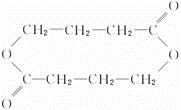 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
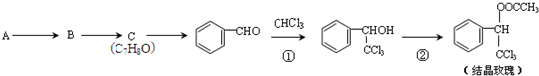
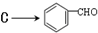 的反应类型是氧化反应,A的结构简式为
的反应类型是氧化反应,A的结构简式为 .
.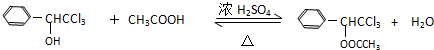 ,反应类型是酯化反应.
,反应类型是酯化反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子核内有10个中子的氧原子:${\;}_{8}^{18}$O | |
| B. | NH4Cl的电子式为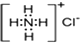 | |
| C. | 羟基的电子式: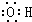 | |
| D. | 乙醇的分子式:CH3CH2OH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
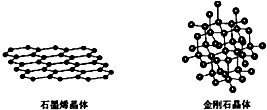
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
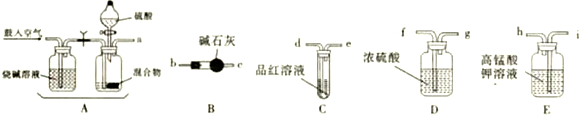
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 芥子气不是烃的衍生物 | |
| B. | 芥子气可以和硝酸银溶液反应生成氯化银沉淀 | |
| C. | S2Cl2中有极性键和非极性键 | |
| D. | NaOH溶液解毒原理是酸碱中和反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com