
| A. | 0.1s | B. | 2.5s | C. | 5s | D. | 10s |
分析 同一可逆反应中,同一时间段内各物质的反应速率之比等于其计量数之比,在这段时间内用O2表示的反应速率为0.01mol•L-1•s-1,则三氧化硫的反应速率为0.02mol•L-1•s-1,根据v=$\frac{△c}{△t}$计算反应时间.
解答 解:同一可逆反应中,同一时间段内各物质的反应速率之比等于其计量数之比,在这段时间内用O2表示的反应速率为0.01mol•L-1•s-1,则三氧化硫的反应速率为0.02mol•L-1•s-1,根据v=$\frac{△c}{△t}$得反应时间=$\frac{△c}{v}$=$\frac{0.2mol/L}{0.02mol/(L.s)}$=10s,故选D.
点评 本题考查化学反应速率有关计算,明确化学反应速率与其计量数的关系是解本题关键,题目难度不大.


 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:选择题
| A. | 5n-12 | B. | 3n-12 | C. | 3n-6 | D. | n-10 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由三氯化铁到氢氧化铁胶体有发生化学变化发生 | |
| B. | 氢氧化铁胶体溶液的颗粒的直径在10-9~10-7m之间 | |
| C. | 可以用丁达尔效应实验有效鉴别氯化钠溶液和氢氧化铁溶液 | |
| D. | 三氯化铁可用作净水剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3.2gO2和O3混合气体所含的氧原子总数为0.2NA | |
| B. | 一定条件下,2 mol SO2和1mol O2在密闭容器中充分反应后,容器内气体分子总数为2NA | |
| C. | 12g金刚石含4NA个C-C键 | |
| D. | 0.1 mol Na在空气中完全燃烧生成Na2O2,转移的电子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
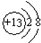 .
.| 选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
| A | 铁是地壳中含量最高的金属元素 | 铁是人类最早使用的金属材料 | Ⅰ对;Ⅱ对. |
| B | 铝箔在酒精灯火焰上加热融化但不滴落 | 铝箔对熔化的铝有较强的吸附作用 | Ⅰ对;Ⅱ错. |
| C | 铝粉可以和氧化铁粉末发生铝热反应 | 铝热反应是工业炼铁最常用方法 | Ⅰ对;Ⅱ错. |
| D | 铜在潮湿空气中表面会生成铜绿 | 可用铜容器盛放浓硫酸 | Ⅰ对;Ⅱ对. |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
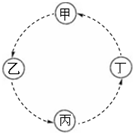 甲、乙、丙、丁的相互转化关系如图所示(部分反应物及反应条件已略去,箭头表示一步转化).下列各组物质中,不能满足图示转化关系的是( )
甲、乙、丙、丁的相互转化关系如图所示(部分反应物及反应条件已略去,箭头表示一步转化).下列各组物质中,不能满足图示转化关系的是( )| 甲 | 乙 | 丙 | 丁 | |
| A | Fe | FeCl3 | Fe (OH)3 | Fe2O3 |
| B | NaAlO2 | Al (OH)3 | Al2O3 | Al |
| C | Na | Na2O2 | Na2CO3 | NaCl |
| D | SiO2 | H2SiO3 | Na2SiO3 | Si |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
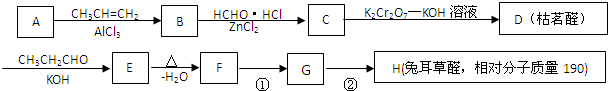
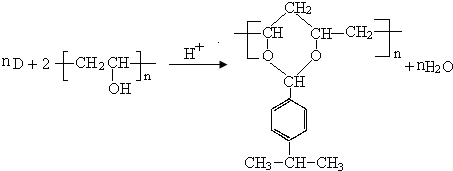
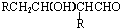 $→_{-H_{2}O}^{△}$
$→_{-H_{2}O}^{△}$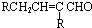
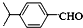 .
.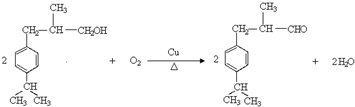 .
.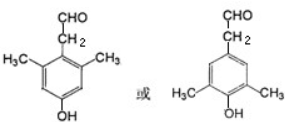 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com