
| A、若甲乙两气体质量相同,则甲乙两气体分子数一定相同 |
| B、若甲的相对分子质量比乙小,则甲的密度比乙的密度大 |
| C、若甲乙两气体的体积相同,则甲乙两气体的原子数一定相同 |
| D、甲乙两种气体的气体摩尔体积一定相同 |
| m |
| M |
| m |
| M |
| V |
| Vm |


 小题狂做系列答案
小题狂做系列答案科目:高中化学 来源: 题型:

| n(H2) |
| n(CO) |
| n(H2) |
| n(CO) |
| n(Mn) |
| n(Cu) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、已知2SO2+O2?2SO3的正反应为放热反应,则SO2的能量一定高于SO3的能量 |
| B、热化学方程式前面的化学计量数代表分子个数 |
| C、S(s)+O2(g)═SO2(g)△H1;S(g)+O2(g)═SO2(g)△H2,则△H1<△H2 |
| D、已知2C(s)+2O2(g)═2CO2(g)△H1;2C(s)+O2(g)═2CO(g)△H2,则△H1<△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、氯离子的结构示意图: | ||
B、作为相对原子质量测定标准的碳核素:
| ||
C、氯化镁的电子式: | ||
D、用电子式表示氯化氢分子的形成过程: + + → →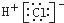 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.12L SO2含有的氧原子数目为0.1NA |
| B、常温常压下,14g N2含有7NA个电子 |
| C、0.1mol?L-1的MgCl2溶液中Cl-离子数为0.2NA |
| D、1mol氯气参加氧化还原反应时电子转移为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、lH、2H、3H为同素异形体 |
| B、lH、2H、3H的中子数相同 |
| C、lH、2H、3H互为同位素 |
| D、lH、2H、3H的质量数相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com