
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗高锰酸钾溶液体积/mL | 10.32 | 10.02 | 9.98 |
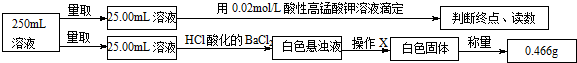
分析 (1)称取3.920g摩尔盐样品,需要电子天平,精确到0.0001g,配制250mL溶液过程中需要精确定量仪器250ml容量瓶;
(2)加入KSCN溶液是检验铁离子的试剂,遇到铁离子会生成血红色溶液,无明显现象说明无铁离子,证明盐中为亚铁离子,亚铁离子在空气中被氧气氧化生成氢氧化铁红褐色沉淀;
(3)步骤④中白色悬浊液得到白色固体,分离试验方法为过滤、洗涤、干燥等步骤;
(4)碘单质氧化性弱不能氧化亚铁离子;
(5)待测液久置,会导致空气中氧气氧化亚铁离子,消耗标准溶液高锰酸钾溶液体积减小;
(6)根据题中实验步骤及数据可知,滴定亚铁离子用去的高锰酸钾溶液的体积的数据中,第一次误差较大,为偶然误差应去掉,所以高锰酸钾溶液的体积为$\frac{10.02+9.98}{2}$mL=10.00mL,根据高锰酸钾的物质的量可以确定亚铁离子的物质的量,根据白色固体0.4660g可以确定硫酸根离子的物质的量,利用电荷守恒可知铵根离子的物质的量,由样品的质量及硫酸根离子、亚铁离子及铵根离子的质量确定结晶水的质量,据此可确定摩尔盐的组成.
解答 解:(1)配制摩尔盐溶液时,称取3.9200g摩尔盐样品要用电子天平称取,根据装置图可知,配制250mL溶液定容时要用250mL容量瓶,
故答案为:电子天平;250mL容量瓶;
(2)②取少量配制溶液,加入KSCN溶液,无明显现象,证明无铁离子存在,确定红褐色沉淀中的铁元素在摩尔盐中是以亚铁离子形式存在,产生红褐色沉淀的离子方程式为:4Fe2++8OH-+O2+2H2O=4Fe(OH)3↓,
故答案为:确定红褐色沉淀中的铁元素在摩尔盐中是以亚铁离子形式存在;4Fe2++8OH-+O2+2H2O=4Fe(OH)3↓;
(3)根据实验二③中操作流程可知,白色悬浊液为硫酸钡,要精确称量硫酸钡的质量要经过过滤、洗涤、干燥再称量,
故答案为:过滤、洗涤、干燥或烘干(冷却);
(4)步骤④中酸性高锰酸钾溶液不能用碘的酒精溶液代替,因为碘单质和亚铁离子不发生反应,不能测定实验,
故答案为:不能;碘单质与亚铁离子不反应;
(5)步骤④若在滴定过程中,待测液久置,空气中氧气氧化亚铁离子,消耗标准溶液高锰酸钾溶液体积减小,c(待测)=$\frac{c(标准)V(标准)}{V(待测)}$可知测定亚铁离子减小,
故答案为:偏小;
(6)根据题中实验步骤及数据可知,滴定亚铁离子用去的高锰酸钾溶液的体积的数据中,第一次误差较大,为偶然误差应去掉,所以高锰酸钾溶液的体积为$\frac{10.02+9,98}{2}$mL=10.00mL,高锰酸钾的物质的量为0.02mol/L×0.01L=0.0002mol,根据反应MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O,可知3.9200g摩尔盐样品中亚铁离子的物质的量为0.0002mol×$\frac{250}{25}$×5=0.01mol,其质量为0.5600g,白色固体硫酸钡为0.4660g,所以3.9200g摩尔盐样品中硫酸根离子的物质的量为$\frac{0.4660g}{233g/mol}$×$\frac{250}{25}$=0.02mol,其质量为1.9200g,根据电荷守恒可知3.9200g摩尔盐样品中铵根离子的物质的量为0.02mol×2-0.01mol×2=0.02mol,其质量为0.3600g,所以样品中结晶水物质的量为$\frac{3.9200g-1.9200g-0.5600g-0.3600g}{18g/mol}$=0.06mol,所以摩尔盐的组成为(NH4)2SO4•FeSO4•6H2O或(NH4)2Fe(SO4)2•6H2O,
故答案为:(NH4)2SO4•FeSO4•6H2O或(NH4)2Fe(SO4)2•6H2O.
点评 本题考查了物质组成和结构的实验测定过程分析,主要是物质性质、滴定实验、化学式组成计算等知识点,题目难度中等.


科目:高中化学 来源: 题型:解答题
 其中含有的化学键的类型离子键、共价键
其中含有的化学键的类型离子键、共价键查看答案和解析>>
科目:高中化学 来源: 题型:解答题
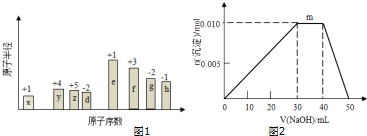
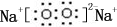 ,0.10mol该化合物与足量水反应时转移的电子数为6.02×1022.
,0.10mol该化合物与足量水反应时转移的电子数为6.02×1022.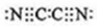 ,(yz)2称为拟卤素,性质与卤素类似,其与氢氧化钠溶液反应的化学方程式是2NaOH+(CN)2=NaCN+NaCNO+H2O.
,(yz)2称为拟卤素,性质与卤素类似,其与氢氧化钠溶液反应的化学方程式是2NaOH+(CN)2=NaCN+NaCNO+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
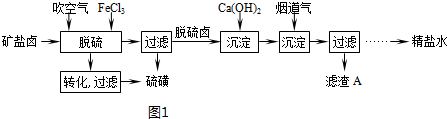
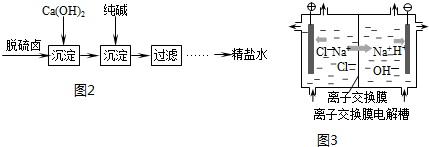
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 发酵粉就是NaHCO3,使用它可使生产的食品疏松可口 | |
| B. | 燃煤中添加适量的CaO,有利于降低酸雨形成的概率 | |
| C. | 放置较久的红薯比新挖出土的甜,可能与葡萄糖的水解有关 | |
| D. | 用液溴来吸收香蕉产生的乙烯,达到保鲜的目的 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com