
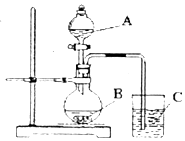
 某研究性学习小组设计了一组实验验证元素周期律.
某研究性学习小组设计了一组实验验证元素周期律.分析 (Ⅰ)(1)根据生成气体的剧烈程度判断金属性强弱,镁条表面有氧化镁,反应现象不明显;
(2)根据氢氧化镁、氢氧化铝是否溶于强碱设计;
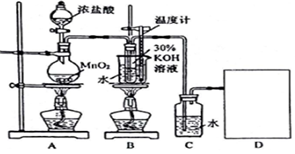
(Ⅱ)(1)利用强酸制备弱酸进行,A是强酸,常温下可与铜反应,为硝酸;B是块状固体,打开分液漏斗的活塞后,C中可观察到白色沉淀生成,则B为碳酸钙、C为硅酸钠;
(2)烧杯中二氧化碳与硅酸钠溶液反应生成硅酸和碳酸钠(或碳酸氢钠);
(3)硝酸易挥发,制备的二氧化碳中含有硝酸,干扰了检验结果.
解答 解:(Ⅰ)(1)根据生成气体的剧烈程度判断金属性强弱,镁条表面有氧化镁,未除去镁表面的氧化膜,反应现象不明显,
故答案为:未除去镁表面的氧化膜;
(2)根据氢氧化镁、氢氧化铝是否溶于强碱设计,具体方法:取镁、铝的可溶盐逐滴加氢氧化钠溶液均产生氢氧化物沉淀,过量碱液可使生成的Al(OH)3溶解,而Mg(OH)2则不溶,
故答案为:取镁、铝的可溶盐逐滴加氢氧化钠溶液均产生氢氧化物沉淀,过量碱液可使生成的Al(OH)3溶解,而Mg(OH)2则不溶;
(Ⅱ)(1)利用强酸制备弱酸进行,A是强酸,常温下可与铜反应,A是硝酸;B是块状固体,打开分液漏斗的活塞后,C中可观察到白色沉淀生成,则B为CaCO3、C为硅酸钠或硅酸钾,
故答案为:CaCO3;
(2)二氧化碳可与硅酸钠反应生成硅酸,且生成碳酸钠,如二氧化碳过量,可生成碳酸氢钠,反应的离子方程式为:CO2+SiO32-+H2O=H2SiO3↓+CO32- 或:2CO2+SiO32-+2H2O=H2SiO3↓+2HCO3-,
故答案为:CO2+SiO32-+H2O=H2SiO3↓+CO32- 或:2CO2+SiO32-+2H2O=H2SiO3↓+2HCO3-;
(3)硝酸易挥发,生成的二氧化碳气体中含有硝酸,干扰了检验结果,所以该实验的不足之处是未除去CO2气体中的硝酸,
故答案为:未除去CO2气体中的硝酸.
点评 本题考查了性质方案的设计,题目难度中等,涉及元素周期律应用、元素推断、离子方程式书写、实验方案的设计等知识,明确实验原理为解答关键,注意掌握化学实验方案的设计原则,试题培养了学生的分析能力及化学实验能力.


科目:高中化学 来源: 题型:实验题
| 实验 编号 | 试剂及其用量 | |||
| 0.2mol•L-1kJ/mL | KClO3(s)/g | 6.0mol•L-1H2SO4/mL | H2O/mL | |
| 1 | 1.0 | 0.1 | 0 | a |
| 2 | 1.0 | 0.1 | 3.0 | b |
| 3 | 1.0 | 0.1 | 6.0 | c |
| 4 | 1.0 | 0.1 | 9.0 | 0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
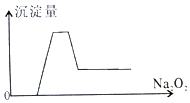 有一透明溶液,取出少量滴入BaCl2溶液,有白色沉淀生成;另取一定体积的该溶液加入过量Na2O2,有无色有刺激性味气体产生,同时有白色沉淀生成,其沉淀量(纵坐标)与加入Na2O2的量(横坐标)的关系如图所示,根据以上判断在该溶液中一定存在的离子是( )
有一透明溶液,取出少量滴入BaCl2溶液,有白色沉淀生成;另取一定体积的该溶液加入过量Na2O2,有无色有刺激性味气体产生,同时有白色沉淀生成,其沉淀量(纵坐标)与加入Na2O2的量(横坐标)的关系如图所示,根据以上判断在该溶液中一定存在的离子是( )| A. | ①②③④⑦ | B. | ①③④⑦ | C. | ①②③⑤⑦ | D. | ①③④⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该工艺中MgO可循环利用 | |
| B. | 理论上 1mol NH4Cl制得Cl2的体积一定为11.2L | |
| C. | 在800~1000℃条件下,O2的还原性强于Cl2的还原性 | |
| D. | 若反应2NH3+MgCl2+H2O═2NH4Cl+MgO能自发进行,则该反应△H>0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 制作航天服的聚酯纤维和用于光缆通信的光导纤维都是新型无机非金属材料 | |
| B. | “青蒿一握,以水二升渍,绞取汁”,屠呦呦对青蒿素的提取属于物理变化 | |
| C. | 在食品袋中放入盛有硅胶和铁粉的透气小袋,分别可防止食物受潮、氧化变质 | |
| D. | 采用“静电除尘”“燃煤固硫”、“汽车尾气催化净化”可提高空气质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
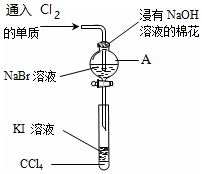 为了验证VIIA族部分元素非金属性递变规律,设计如图进行实验,
为了验证VIIA族部分元素非金属性递变规律,设计如图进行实验,查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纯银物品久置表面变暗 | |
| B. | 生铁(含有碳等杂质)比纯铁在潮湿的环境中容易生锈 | |
| C. | 铁质器件附有铜质配件,在接触处易生铁锈 | |
| D. | 黄铜(铜锌合金)制作的铜锣不易产生铜绿 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2S溶液中只存在2个电离平衡 | |
| B. | c(OH-)=$\sqrt{{K}_{w}}$的溶液一定呈中性 | |
| C. | 加热碳酸钠溶液可证明其水解是吸热反应 | |
| D. | 常温下,在AlPO4和FePO4的饱和溶液中滴加少量Na3PO4溶液,Ksp(AlPO4)和Ksp(FePO4)将减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度 | 1760℃ | 2400℃ | 2730℃ |
| 平衡常数 | 2.4×10-4 | 6.4×10-3 | 8.9×10-3 |
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/10-4mol/L | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
| c(CO)/10-3mol/L | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com