
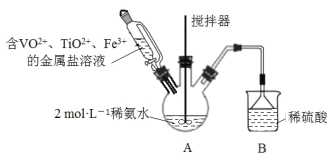
【题目】钒基固溶体合金是一类重要的贮氢材料。某课外小组采用廉价原料 NH4VO3、TiO2 和 Fe2O3,制出含 VO2+、TiO2+和 Fe3+的金属盐溶液,然后选择氨水作沉淀剂进行共沉淀反应(有 氨气逸出),对共沉淀物[含 VO(OH)2、Ti(OH)4、Fe(OH)3]进行煅烧还原制备合金样品。制备共沉 淀物的装置如图:
(1)实验中用浓氨水配制 500mL 2 mol·L-1 的稀氨水,需用到的玻璃仪器有烧杯、胶头滴管、玻璃 棒和_____、_____。
(2)装置 B 的作用是_________________________________________________。
(3)制备 VO2+时,用草酸(H2C2O4)将 VO2+还原得 VO2+。若把草酸改为盐酸,也能得到 VO2+, 但会产生一种有毒气体,该反应的离子方程式为_____。
(4)反应过程需控制温度为 60℃,三颈烧瓶的加热方式是_________________。
(5)往三颈烧瓶中滴加含金属离子的混合液,得悬浊液,取出充分沉降。
①检测上层清液是否含 Fe3+的实验方案是___________。
②经过滤、无水乙醇洗涤、低温干燥,得共沉淀物。使用无水乙醇洗涤的优点是_____。
【答案】500 ml容量瓶 量筒 吸收尾气中的氨气并防止倒吸 2VO2++4H+ +2C1- =2VO2+ +2H2O+Cl2↑ 水浴加热 取少量上层清液与试管中,加入KSCN溶液,观察溶液是否变成血红色 乙醇易挥发容易干燥,减少洗涤时因固体溶解而损失
【解析】
(1)实验中用浓氨水配制 500mL 2 mol·L-1的稀氨水,需要用量筒量取浓氨水的体积,在烧杯中用玻璃棒搅拌溶解,冷却后,用玻璃棒引流转移至500ml容量瓶,用蒸馏水洗涤烧杯和玻璃棒两到三次,洗涤液转移至500 ml容量瓶,要用胶头滴管进行定容。需用到的玻璃仪器有烧杯、胶头滴管、玻璃棒、500 ml容量瓶和量筒,
答案为:500 ml容量瓶;量筒;
(2)选择氨水作沉淀剂进行共沉淀反应(有氨气逸出),装置 B 的作用是吸收尾气中的氨气并防止倒吸,
答案为:吸收尾气中的氨气并防止倒吸;
(3由信息可知盐酸将VO2+还原为VO2+ ,还生成氯气,由电子守恒、电荷守恒及原子守恒可知离子反应为2VO2++4H+ +2C1- =2VO2+ +2H2O+Cl2↑,答案为:2VO2++4H+ +2C1- =2VO2+ +2H2O+Cl2↑;
(4)反应过程需控制温度为60°C ,三颈烧瓶的加热方式应该为60°C水浴加热,
答案为:水浴加热;
(5)①检测上层清液是否含Fe3+的实验方案是取少量上层清液与试管中,加入KSCN溶液,观察溶液是否变成血红色,故答案为:取少量上层清液与试管中,加入KSCN溶液,观察溶液是否变成血红色;
②使用无水乙醇洗涤的优点是乙醇易挥发容易干燥、减少洗涤时因固体溶解而损失,
故答案为:乙醇易挥发容易干燥,减少洗涤时因固体溶解而损失。


 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:
【题目】化合物G是一种芳香酯类物质,也是一种重要的香料,工业上合成它的一种方法如下图所示。图中D的相对分子质量为106,D、E的核磁共振氢谱均只有两个峰,B经过氧化可以得到C。

已知:![]() R1CHO+HCOOH+R2CHO(R1、R2是烃基或者氢原子)。
R1CHO+HCOOH+R2CHO(R1、R2是烃基或者氢原子)。
(1)A的结构简式为___________________________,D的名称是___________________。
(2)D→E的反应类型为_______________,“一定条件”的内容是__________________。
(3)B中官能团的名称是__________,G的结构简式为___________________________。
(4)E→F的化学方程式为_________________。
(5)符合下列条件的F的同分异构体共有________种,写出一种核磁共振氢谱有5个峰的同分异构体的结构简式:________________________________。
①遇FeCl3溶液能发生显色反应 ②含有醚键
(6)写出以乙烯为原料合成HCOOCH2CH2OOCH的合成路线(无机试剂任选,合成路线参照题中的书写形式)________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向100 mL NaOH溶液中通入一定量的CO2气体,充分反应后,再向所得溶液中逐滴加入0.2 mol·L-1的盐酸,产生CO2的体积与所加盐酸体积之间关系如图所示。下列判断正确的是( )

A. 原NaOH溶液的浓度为0.2 mol·L-1
B. 通入CO2在标准状况下的体积为448 mL
C. 所得溶液的溶质成分的物质的量之比为n(NaOH)∶n(Na2CO3)=1∶3
D. 所得溶液的溶质成分的物质的量之比为n(NaHCO3)∶n(Na2CO3)=1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中的一定量的混合气体发生反应:xA(g)+yB(g)![]() zC(g)平衡时测得C的浓度为1 mol·L-1,保持温度不变,将容器的容积扩大到原来的2倍,再达到平衡时,测得C的浓度为0.6 mol·L-1,下列有关判断正确的是( )
zC(g)平衡时测得C的浓度为1 mol·L-1,保持温度不变,将容器的容积扩大到原来的2倍,再达到平衡时,测得C的浓度为0.6 mol·L-1,下列有关判断正确的是( )
A. x+y>zB. 平衡向逆反应方向移动
C. B的转化率降低D. A的体积分数减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上利用如下反应制取P4:2Ca(PO4)2 +6SiO2+10C![]() 6CaSiO3+P4+10CO
6CaSiO3+P4+10CO
回答下列问题:
(1)基态硅原子的核外电子排布式为___。
(2)Si、P、S元素第一电离能大小关系为___。
(3)P4中P原子的杂化方式是___ ,P4的空间结构为___ ,键角∠PPP=___。
(4)与CO互为等电子的阴离子是___ (填化学式)。
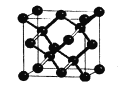
(5)晶体硅与金刚石结构相似,下图为晶体硅的晶胞结构。已知硅原子的半径为r nm,晶体硅的密度是___g/cm3。
(6)硅的含氧化合物都以硅氧四面体(SiO4)作为基本结构单元,如图a所示,可简化为图b。
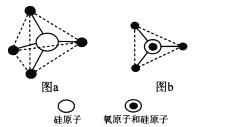
硅、氧原子通过共用氧原子形成各种不同的硅酸根负离子,如图c和图d,图c的化学式____________。在无限长链的硅酸根中硅氧原子之比为____。
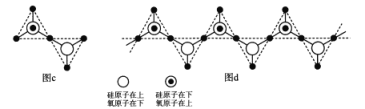
硅、氧原子除可形成长链外,也可形成层状和立体网状结构。在立体网状结构中,硅、氧原子数之比为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用O2氧化NH3制备硝酸的装置如图所示(夹持装置略),下列说法不正确的是
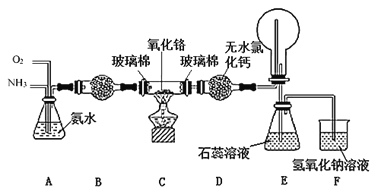
A.球形干燥管B中可以填充碱石灰或五氧化二磷
B.实验过程中,若熄灭酒精灯,装置C中的氧化铬继续保持红热,说明装置C中的反应放热
C.球形干燥管D中的无水氯化钙可吸收尾气中的氨气和水蒸气
D.装置E中的石蕊试液最终变红,说明锥形瓶中有硝酸产生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.节日里燃放的五彩缤纷的烟花是某些金属元素化学性质的展现
B.用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热,熔化后的液态铝滴落下来,说明金属铝的熔点较低
C.将等物质的量的氧化钠和过氧化钠分别投入到足量且等质量的水中,得到溶质质量分数分别是a%和b%的两种溶液,则a和b的关系是a=b
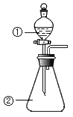
D.用如图装置进行实验,将装置①中的AlCl3溶液滴入装置②浓氢氧化钠溶液,溶液中可观察到有大量白色沉淀产生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】普通水泥在固化过程中其自由水分子减少并形成碱性溶液。根据这一物理化学特点,科学家发明了电动势法测水泥的初凝时间。此法的原理如图所示,反应的总方程式为2Cu+Ag2O===Cu2O+2Ag,下列有关说法正确的是 ( )

A. 2 mol Cu与1 mol Ag2O的总能量低于1 mol Cu2O与2 mol Ag具有的总能量
B. 负极的电极反应式为2Cu+2OH--2e-===Cu2O+H2O
C. 测量原理示意图中,电流方向从Cu→Ag2O
D. 电池工作时,OH-向正极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
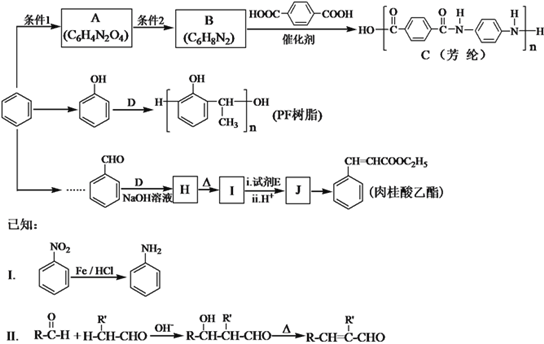
【题目】苯是一种非常重要的化工原料,利用苯可以合成多种有机物。有人设计了合成芳纶、PF树脂和肉桂酸乙酯的路线,如下图:
 回答下列问题:
回答下列问题:
(1)反应条件1是____________。
(2)B分子中的官能团的名称为_________,B→C的反应类型为____________。
(3)D的结构简式为________,生成PF树脂的化学方程式为_______________。
(4)试剂E是_________。
(5)由J合成肉桂酸乙酯的化学方程式为 _____________________。
(6)写出同时满足下列条件的肉桂酸乙酯的一种同分异构体__________。
①苯环上仅有2个取代基且处于对位
②能发生水解反应和银镜反应,其中一种水解产物遇FeCl3溶液显色
③存在顺反异构
(7)以D为原料,选用必要的无机试剂合成乙二醛,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上或下注明试剂和反应条件)。_____________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com