
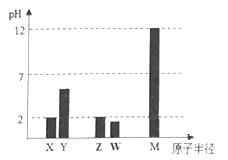
【题目】X、Y、Z、W、M为短周期主族元素,25°C时,其最高价氧化物对应的水化物(浓度均为 0.01mol·L-1)溶液的pH和原子半径的关系如图所示。下列有关说法不正确的是
A. 最简单气态氢化物的热稳定性:Z>W
B. Y的最高价氧化物的电子式为:![]()
C. W的气态氢化物是强酸
D. X、M两种元素形成的简单离子半径大小顺序:X>M
【答案】C
【解析】
X、Y、Z、W、M 均为常见的短周期主族元素,由常温下,其最高价氧化物对应的水化物溶液(浓度均为 0.01mol·L-1)的pH,X的pH=2,为一元强酸,则为硝酸,X为N元素,Y的半径大于N,且酸性较硝酸弱,应为C元素;Z的原子半径大于C,Z的最高价含氧酸为一元强酸,则Z为Cl,W的原子半径大于Cl,且对应的酸的pH小于2,应为硫酸,W为S元素;M的原子半径最大,且0.01mol·L-1W的最高价氧化物对应的水化物溶液的pH为12,可知W为Na,以此解答该题。
由以上分析可知X、Y、Z、W、M分别为N、C、Cl、S、Na。
A. Z、W为Cl、S,氯化氢比硫化氢稳定,最简单气态氢化物的热稳定性:Z>W,故A正确;
B. Y为C,Y的最高价氧化物的电子式为:![]() ,故B正确;
,故B正确;
C. W为硫,W的气态氢化物硫化氢是弱酸,故C错误;
D. X、M 简单离子具有相同的核外电子排布,核电荷数越大,离子半径越小,故D正确;
故选C。


 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案科目:高中化学 来源: 题型:
【题目】某化学兴趣小组进行两组电解实验。
实验一:已知固体电解质只有特定离子才能移动。按照下图装置研究α-AgI固体电解质导体是Ag+导电还是I-导电;

实验二:用惰性电极电解硫酸铜和盐酸混合液,对产生的气体进行研究。
关于以上实验,下列说法正确的是
A. 实验一:若α-AgI固体是Ag+导电,则通电一段时间后的晶体密度不均匀
B. 实验一:若α-AgI固体是I-导电,则通电一段时间后的晶体密度仍均匀
C. 实验二:若阳极为纯净气体,阴、阳两极产生的气体体积比可能≥1
D. 实验二:若阳极为混合气体,阴、阳两极产生的气体体积比可能≥1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列生活中常见物质主要成分的化学式表示正确的是( )
A.铁红—Fe2O3B.漂白粉—NaClO
C.生石灰—Ca(OH)2D.纯碱—NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(物质结构与性质)钛呈银白色,因它坚硬、强度大、耐热、密度小,被称为高技术金属。目前生产钛采用氯化法,即将金红石或钛铁矿与焦炭混合,通入氯气并加热制得TiCl4:2FeTiO3+7Cl2+6C![]() 2TiCl4+2FeCl3+6CO; TiO2+2Cl2+2C
2TiCl4+2FeCl3+6CO; TiO2+2Cl2+2C![]() TiCl4+2CO
TiCl4+2CO
将TiCl4蒸馏并提纯,在氩气保护下与镁共热得到钛:TiCl4+2Mg![]() Ti+2MgCl2
Ti+2MgCl2
MgCl2和过量Mg用稀盐酸溶解后得海绵状钛,再在真空熔化铸成钛锭。请回答下列问题:
(1)基态钛原子的价电子排布式为 。
(2)与CO互为等电子体的离子为 (填化学式)。
(3)在CH2Cl2、C6H6、CO2、C2H4中,碳原子采取sp1杂化的分子有 。
(4)TiCl4在常温下是无色液体,在水或潮湿空气中易水解而冒白烟。则TiCl4属于 (填“原子”、“分子”或“离子”)晶体。
(5)与钛同周期的另一种元素钴(Co)可形成分子式均为Co(NH3)5BrSO4的两种配合物,其中一种化学式为[Co(NH3)5Br]SO4,往其溶液中加BaCl2溶液时,现象是 ;往另一种配合物的溶液中加入BaCl2溶液时,无明显现象,若加入AgNO3溶液时,产生淡黄色沉淀,则第二种配合物的化学式为 。
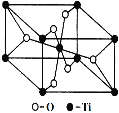
(6)在自然界中TiO2有金红石、板钛矿、锐钛矿三种晶型,其中金红石的晶胞如右图所示,则其中Ti4+的配位数为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期的三种元素X、Y、Z,已知X元素的原子最外只有一个电子,Y元素的原子M层上的电子数是它K层和L层电子总数的一半,Z元素原子的L层上的电子数比Y元素原子的L层上的电子数少2个,则这三种元素所组成的化合物的化学式不可能的是( )
A. X3YZ4 B. X3YZ3 C. X2YZ4 D. X4Y2Z7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某强酸性溶液X可能含有Fe2+、A13+、NH4+、CO32-、SO32-、SO42-、C1-中的若干种,现取X溶液进行连续实验,实验过程及产物如图.说法正确的是

A. X中肯定存在Fe2+、A13+、NH4+、SO42- B. X中不能确定的离子是 A13+和C1-
C. 沉淀I一定是Al(OH)3 D. 溶液E和气体F不能发生化学反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列试剂的保存方法错误的是( )
A.少量的钠保存在煤油中
B.亚硫酸钠固体密封保存
C.保存氯化亚铁溶液时加入铜粉以防止氧化
D.浓硝酸保存在棕色试剂瓶中并置于冷暗处
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组的同学设计了如下装置进行试验探究,请回答下列问题:

(1)为准确读取量气管的读数,除视线应与量气管凹液面最低处向平,还应注意 。若考虑分液漏斗滴入烧瓶中液体的体积(假设其它操作都正确),则测得气体的体积将 (填“偏大”、“偏小”或“无影响”)。
(2)若在烧瓶中放入生铁,用此装置验证生铁在潮湿空气中发生吸氧腐蚀。
①通过分液漏斗向烧瓶中加入的试剂可选用下列 (填序号)
a.NaOH溶液 B.C2H5OH c.NaCl溶液 D.稀硫酸
②能证明生铁在潮湿空气中发生吸氧腐蚀的现象是 。
(2)若烧瓶中放入粗铜片(杂质不参与反应),分液漏斗内放稀硝酸,通过收集并测量NO气体的体积来探究粗铜样品的纯度。你认为此方法是否可行 (填“可行”或“不可行”,若填“不可行”请说明原因)。
(3)为探究MnO2在H2O2制取O2过程中的作用,将等量的H2O2加入烧瓶中,分别进行2次实验(气体体积在同一状况下测定):
序号 | 烧瓶中的物质 | 测得气体体积 |
实验1 | 20 mL H2O2,足量MnO2 | V1 |
实验2 | 20 mL H2O2,足量MnO2和稀硫酸 | V1<V2<2V1 |
若实验1中MnO2的作用是催化剂,则实验2中发生反应的化学方程式为 。
(4)若烧瓶中放入镁铝合金,分液漏斗内放NaOH溶液,分别进行四次实验,测得以下数据(气体体积均已换算成标准状况):
编号 | 镁铝合金质量 | 量气管第一次读数 | 量气管第二次读数 |
Ⅰ | 1.0 g | 10.00 mL | 346.30 mL |
Ⅱ | 1.0 g | 10.00 mL | 335.50 mL |
Ⅲ | 1.0 g | 10.00 mL | 346.00 mL |
Ⅳ | 1.0 g | 10.00 mL | 345.70 mL |
则镁铝合金中镁的质量分数为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com