
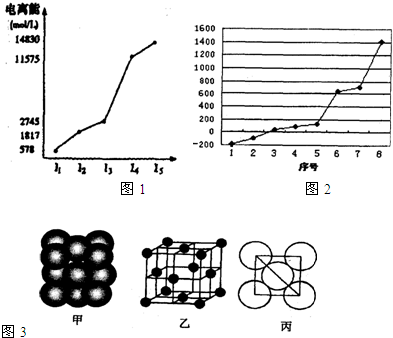
 图表法、图象法是常用的科学研究方法.
图表法、图象法是常用的科学研究方法.
| ||
| 2 |
| 2 |
| 2 |
| 2 |
| m |
| V |
| 1 |
| 8 |
| 1 |
| 2 |
| ||
| 2 |
| 2 |
| 2 |
| 2 |
| 1 |
| 8 |
| 1 |
| 2 |
| M |
| NA |
4×
| ||
16
|
| M | ||
4
|
| M | ||
4
|


 步步高达标卷系列答案
步步高达标卷系列答案科目:高中化学 来源: 题型:
| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物 质 | X | Y | Z | Q |
| 反应前质量/g | 2 | 2 | 84 | 5 |
| 反应后质量/g | 待测 | 24 | 0 | 14 |
| A、化合反应 | B、置换反应 |
| C、分解反应 | D、复分解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,33.6LH2O含有9.03×1023个H2O分子 |
| B、5.6g铁与足量的稀硫酸反应失去电子数为0.3NA个 |
| C、14g氮气中含有7NA个电子 |
| D、0.5mol/LNa2CO3溶液中含有的Na+数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、只有一种生成物的反应一定是化合反应 |
| B、C2H2、CS2、CH2Cl2都是含有极性键的非极性分子 |
| C、CH4是有机物中含氢量最高的物质 |
| D、较不活泼的金属单质不能还原较活泼金属的阳离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| NaOH |
| △ |
| 淀粉酶 |
| 酒化酶 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,22.4L的H2和CO2混合气体中含有的分子总数为NA |
| B、常温常压下,24g金属镁变为镁离子时得到的电子数为2NA |
| C、标准状况下,5.6L水含有的分子数为0.25NA |
| D、1 mol Cl2与足量Fe反应,转移的电子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 阳离子 | K+ | Cu2+ | Fe3+ | Al3+ | Fe2+ | ||||||||
| 阴离子 | Cl- | CO
|
NO
|
SO
|
SiO
|
| 选项 | 污染物 | 处理措施 | 方法类别 |
| A | 废酸 | 加生石灰中和 | 物理法 |
| B | Cu2+等重金属离子 | 加硫酸盐沉降 | 化学法 |
| C | 合复杂有机物的废水 | 通过微生物代谢 | 物理法 |
| D | 碱性的废水 | 用CO2来中和 | 化学法 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com