
【题目】高分子材料PET聚酯树脂和PMMA的合成路线如下: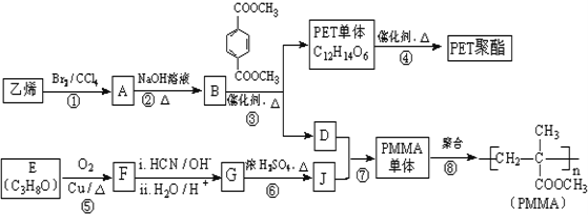
已知:
Ⅰ.RCOOR′+R″18OH ![]() RCO18OR″+R′OH(R、R′、R″代表烃基)
RCO18OR″+R′OH(R、R′、R″代表烃基)
Ⅱ.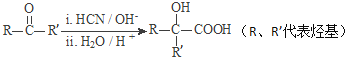
(1)①的反应类型是_____________.
(2)②的化学方程式为_____________.
(3)PMMA单体的官能团名称是_____________、_____________。
(4)F的核磁共振氢谱显示只有一组峰,⑤的化学方程式为_____________。
(5)G的结构简式为_____________。
(6)下列说法正确的是_____________(填字母序号).
a.⑦为酯化反应
b.B和D互为同系物
c.D的沸点比同碳原子数的烷烃高
d.1mol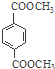 与足量NaOH溶液反应时,最多消耗4molNaOH
与足量NaOH溶液反应时,最多消耗4molNaOH
(7)写出由PET单体制备PET聚酯(化学式为C10nH8nO4n或C10n+2H8n+6O4n+2)并生成B的化学方程式_____________。
【答案】(1)加成反应; (2)![]() ;
;
(3)碳碳双键和酯基;(4)![]() ;
;
(5)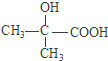 ;(6)ac;
;(6)ac;
(7)
【解析】
试题分析:根据题中各物质转化关系,由PMMA的结构可知,PMMA单体为CH2=C(CH3)COOCH3,E氧化得F,F的核磁共振氢谱显示只有一组峰,F发生信息Ⅱ中的反应得G,G在浓硫酸作用下发生消去反应得J,结合PMMA单体的结构和E的分子式可知,E为CH3CHOHCH3,F为CH3COCH3,G为(CH3)2COHCOOH,J为CH2=C(CH3)COOH,所以D为HOCH3,乙烯与溴发生加成反应生成A为BrCH2CH2Br,A在碱性条件下水解得B为HOCH2CH2OH,B与对苯二甲酸甲酯发生取代反应生成PET单体为 ,PET单体发生信息Ⅰ的反应得PET聚酯。
,PET单体发生信息Ⅰ的反应得PET聚酯。
(1)根据上面的分析可知,反应①的反应类型是加成反应,故答案为:加成反应;
(2)②的化学方程式为 ![]() ,故答案为:
,故答案为:![]() ;
;
(3)PMMA单体为CH2=C(CH3)COOCH3,PMMA单体的官能团名称是碳碳双键和酯基,故答案为:碳碳双键和酯基;
(4)反应⑤的化学方程式为![]() ,故答案为:
,故答案为:![]() ;
;
(5)G的结构简式为  ,故答案为:
,故答案为: ;
;
(6)a.⑦为CH2=C(CH3)COOH与HOCH3发生酯化反应,故a正确;b.D为HOCH3,B为HOCH2CH2OH,它们的羟基的数目不同,所以B和D不是互为同系物,故b错误;c.D中有羟基,能形成氢键,所以D的沸点比同碳原子数的烷烃高,故c正确;d.1mol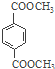 与足量NaOH溶液反应时,最多消耗2molNaOH,故d错误;故选ac;
与足量NaOH溶液反应时,最多消耗2molNaOH,故d错误;故选ac;
(7)由PET单体制备PET聚酯并生成B的化学方程式为 ,故答案为:
,故答案为: 。
。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】合成纤维Z的吸湿性接近于棉花。合成Z的流程图如下所示: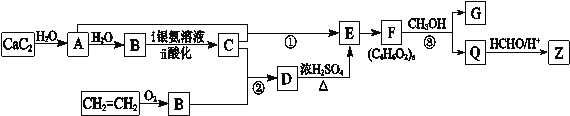
已知:下列反应中R、R′、R″代表烃基
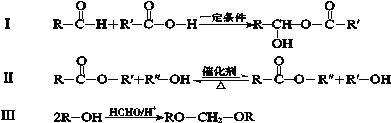
(1)A的结构简式是 。
(2)B的分子式为C2H4O,其官能团的名称是 。
(3)反应①的化学方程式是 。
(4)下列说法正确的是 。(填字母)
a.D→E的反应类型为消去反应 b.D能与Na、NaOH、NaHCO3反应
c.Q分子中含有—OH d.G在酸性或碱性环境中均能水解
(5)E有多种同分异构体,与E具有相同官能团的有 种(含顺反异构体,不包括E),其中核磁共振氢谱有3组吸收峰,且能发生银镜反应的结构简式是 。
(6)合成纤维Z含有六元环状结构,Z的结构简式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于电解质溶液的说法错误的是
A.pH=3的 NH4Cl溶液与pH=3的盐酸中,水电离的c(H+)相等
B.25℃时将0.1mol·L -1 的HF加水不断稀释,![]() 不变
不变
C.K2SO3溶液中加入少量NaOH固体,溶液的pH增大,SO32-水解程度减小
D.pH=5的CH3 COOH 与CH3COONa混合溶液中,c(CH3COO-)<c(Na+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W为四种短周期元素,它们在周期表中位于连续的四个主族,如图所示。Z元素原子最外层电子数是内层电子总数的1/5。下列说法中正确的是
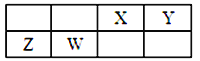
A. 原子半径由小到大的顺序为:X<Z<Y<W
B. Y元素最高价氧化物对应的水化物化学式为H3YO4
C. X、Z两种元素的氧化物中所含化学键类型相同
D. Y最简单气态氢化物比Y相邻周期同主族元素气态氢化物沸点高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表中前两周期的六种元素X、Y、Z、M、N、Q原子序数依次增大,六种元素价电子数之和为26,原子半径依Y、Z、M、N、Q、X依次减小。依据信息,回答下列问题:
(1)Q的核外电子排布图为 。
(2)除X外,其余元素的第一电离能由小到大的顺序为 (用元素符号作答)。
(3)固体A是由以上六种元素中的某些元素组成的离子晶体,结构类似于CsCl,组成中含M元素的质量分数为73.7%,A所有原子的最外层都满足稀有气体原子结构,A受热分解可生成两种单质气体。写出A的电子式 ,常温下A与水反应的化学方程式为 。
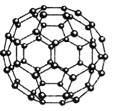
(4)Z元素形成的另一种分子晶体结构如图所示,Z60分子是由60个Z原子构成的,形状酷似足球,有32个面,其中12个面为正五边形,20个面为正六形。Z60分子可与Q元素形成的单质Q2发生加成反应,则加成产物的化学式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫化锌(ZnS)是一种重要的化工原料,难溶于水,可由炼锌的废渣锌灰制取,其工艺流程如图:

(1)为提高锌灰的浸取效率,不采用的方法是______________(填序号)
①研磨②搅拌③多次浸取④升高温度⑤加压
(2)步骤Ⅱ所得滤渣中的物质是______________(写化学式)。
(3)步骤Ⅲ中可得Cd单质,为避免引入新的杂质,试剂b应为______________。
(4)步骤Ⅳ还可以回收Na2SO4来制取Na2S。
①检验ZnS固体是否洗涤干净的方法是______________;
②Na2S可由等物质的量的Na2SO4和CH4在高温、催化剂条件下制取.化学反应方程式为______________。
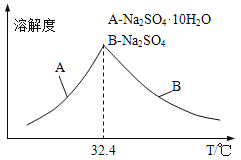
③已知Na2SO410H2O及Na2SO4的溶解度随温度变化曲线如图。从滤液中得到Na2SO410H2O的操作方法是______________。
(5)若步骤Ⅱ加入的ZnCO3为bmol,步骤Ⅲ所得Cd为dmol,最后得到VL、物质的量浓度为cmol/L的Na2SO4溶液.则理论上所用锌灰中含有锌元素的质量为______________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应Fe+H2SO4=FeSO4+H2↑的能量变化趋势,如图所示:
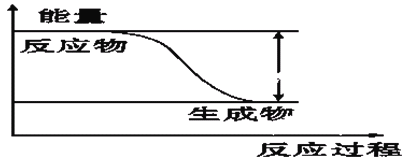
(1)该反应为 反应(填“吸热”或“放热”)。
(2)若要使该反应的反应速率加快,下列措施可行的是 (填字母)。
A.改铁片为铁粉 B.改稀硫酸为98%的浓硫酸 C.升高温度
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜片上产生的现象为 。溶液中SO42-向 极(填“贴片”或“铜片”),外电路中电子 移动。(填“由铁片向铜片”或“由铜片向铁片”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有铁和铜组成的合金共a mol,其中铜的物质的量分数为x。将此合金研成粉末状后全部投入含b mol硝酸的稀溶液中,微热使其充分反应,硝酸的还原产物只有NO。
(1)用粒子符号填写下列空白(列举出全部可能出现的情况):

(2)当溶液中金属离子只有Fe2+、Cu2+时,则b的取值范围为 (用a、x表示)
(3)当x=0.5时,溶液中Fe3+和 Fe2+的物质的量相等,在标准状况下共生成672毫升NO气体,求a= ,b= 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】达比加群酯,是由德国公司开发的新型口服抗凝血药物,针对急性和慢性血栓栓塞性疾病的预防及治疗。F是其合成过程中的重要中间体,以下是F的合成路线图:(-Me表示甲基)

(1)写出A中含氧官能团的名称:_________和__________。
(2)B→C的反应类型是______________________。
(3)写出C→D转化的化学方程式__________________________。
(4)写出符合条件的B的同分异构体的结构简式_________________。
①属于芳香族化合物 ②能发生银镜反应 ③分子中只有两种化学环境不同的氢原子
(5)已知:![]()
肉桂酰氯![]() 是一种重要的合成中间体,试写出以苯甲醇和乙醛为原料合成该化合物的合成路线流程图(无机原料任用)。
是一种重要的合成中间体,试写出以苯甲醇和乙醛为原料合成该化合物的合成路线流程图(无机原料任用)。
合成路线流程图示例如下:
![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com