
广泛存在的含碳化合物
1.含碳化合物
碳元素在自然界中主要以________的形式存在,碳元素是构成化合物种类________的元素.含碳化合物的矿石常见物质如右图:
2.Na2CO3与NaHCO3
(1)碳酸钠俗称________或________,是________固体,广泛用于________等工业;碳酸氢钠俗称________,是________固体,是焙制糕点所用的________的主要成分之一.
(2)Na2CO3和NaHCO3的化学性质
由于Na2CO3、NaHCO3都属于盐,所以Na2CO3能与某些酚、碱、盐反应;NaHCO3也能与某些酸、碱、盐反应.反应的化学方程式为:与酸反应:Na2CO3+2HCl![]() ________.
________.
NaHCO3+HCl![]() ________.
________.
与碱反应:Na2CO3+Ba(OH)2![]() ________.
________.
2NaHCO3+Ba(OH)2![]() ________.
________.
与盐:Na2CO3+BaCl2![]() ________,
________,
NaHCO3+BaCl2![]() ________.
________.
(3)NaHCO3的其他性质——受热分解
NaHCO3热稳定性差,受热发生________;Na2CO3热稳定性好,受热不发生分解反应.
2NaHCO3![]() Na2CO3+________.
Na2CO3+________.
(4)碳酸盐与碳酸氢盐的相互转化
一般说来,碳酸盐能与碳酸(二氧化碳和水)反应转化为________,碳酸氢盐能与碱反应转化为________.
例:
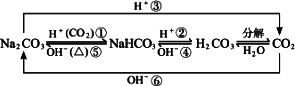
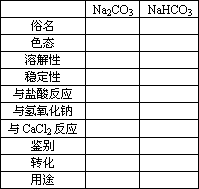
(5)总结:Na2CO3与NaHCO3列表比较
科目:高中化学 来源: 题型:

| ||
| (2)H+ |


 CH2CH2
CH2CH2 )反应合成PBSA的化学方程式:
)反应合成PBSA的化学方程式:| 一定条件 |
 OC-COO(CH2)4O
OC-COO(CH2)4O H+(2n-1)H2O
H+(2n-1)H2O| 一定条件 |
 OC-COO(CH2)4O
OC-COO(CH2)4O H+(2n-1)H2O
H+(2n-1)H2O

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
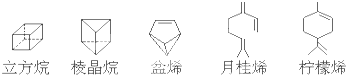
 碳原子的杂化轨道类型为
碳原子的杂化轨道类型为查看答案和解析>>
科目:高中化学 来源:2013-2014学年辽宁省高三上学期期中考试理综化学试卷(解析版) 题型:填空题
金属镍,铁及非金属元素碳在合金材料,有机合成材料中有广泛的应用. 请回答下列问题:
(1)Ni原子的核外电子排布式为 .
(2)Fe原子的外围电子排布图为 .
(3)含碳化合物丙烯腈(H2C=CH—C≡N)分子中碳原子轨道杂化类型为
(4)NiO,FeO的晶体类型均与氯化钠晶体相同,Ni2+和Fe2+离子半径分别为69 Pm和78 Pm,则两种物质的熔点
NiO FeO(填“>”或“<”),判断依据是 .
(5)CaC2晶体的晶胞也与氯化钠相似,但由于CaC2晶体中的C22-存在,使晶胞沿一个方向拉长,则CaC2晶体中1个C22-周围距离最近且相等的Ca2+数目为 ,C22-与O22+互为等电子体,写出O22+的电子式 .
(6)铁在一定条件下可形成体心立方堆积的晶体,设铁原子半径为r,请用含r的代数式表示该晶体空间利用率 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com