
| A. | 硫氰酸钾溶液 | B. | NaOH溶液 | ||
| C. | 新制氯水、硫氰酸钾溶液 | D. | 酸性KMnO4溶液 |
分析 Fe3+的检验方法为:取待测液于试管中,向待测溶液中加入KSCN溶液,溶液立刻变成红色说明溶液中有Fe3+,即Fe3++3SCN-?Fe(SCN)3;根据常见离子的颜色判断Fe3+(黄色);Fe3+与OH-反应生成红褐色Fe(OH)3;
Fe2+的检验方法为:再取待测液于试管中,加KSCN溶液没有明显现象,加入氯水溶液变成红色,说明溶液只有Fe2+;根据常见离子的颜色判断Fe2+(浅绿色);向Fe2+溶液中加入NaOH溶液后,观察到生成的白色沉淀迅速变成灰绿色,最后变成红褐色;Fe2+能使酸性KMnO4溶液褪色,注意混合溶液中亚铁离子检验需要注意现象的相互干扰,据此即可解答.
解答 解:A.KSCN溶液;加入KSCN溶液,发生络合反应,Fe3++3SCN-?Fe(SCN)3溶液立即呈血红色,证明含有三价铁离子,不能说明溶液只有Fe2+,硫氰酸钾溶液不能检验该溶液中存在Fe2+,故A错误;
B.NaOH溶液,向Fe2+溶液中加入NaOH溶液后,Fe2+与OH-反应生成Fe(OH)2,Fe2++2OH-=Fe(OH)2↓,Fe(OH)2不稳定易被氧气氧化为Fe(OH)3,4Fe(OH)2+O2+2H2O=4Fe(OH)3,白色的Fe(OH)2沉淀变成红褐色Fe(OH)3,向Fe2+溶液中加入NaOH溶液后,观察到生成的白色沉淀迅速变成灰绿色,最后变成红褐色;Fe3+与OH-反应Fe3++3OH-=Fe(OH)3↓,生成红褐色Fe(OH)3,两者反应现象干扰,不能检验该溶液中存在Fe2+,故B错误;
C.某溶液中含有Fe3+、Fe2+,加入硫氰酸钾溶液变红色,用新制氯水、硫氰酸钾溶液不能检验溶液中是否存在亚铁离子,故C错误;
D.酸性KMnO4溶液;因为Fe2+具有较强的还原性能使酸性KMnO4溶液褪色,Fe3+不能,故能够用酸性KMnO4溶液鉴别Fe2+和Fe3+,故D正确;
故选D.
点评 本题考查了二价铁离子和三价铁离子的实验检验方法,题目难度不大,注意掌握亚铁离子与铁离子的化学性质及常用的检验方法,试题能够培养学生灵活应用所学知识的能力.


科目:高中化学 来源: 题型:选择题
| A. | 温度相同、体积相同的O2和N2 | B. | 质量相等、密度不等的N2和C2H4 | ||
| C. | 压强相等、温度相等的CO和C2H4 | D. | 压强相同、体积相同的N2和O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
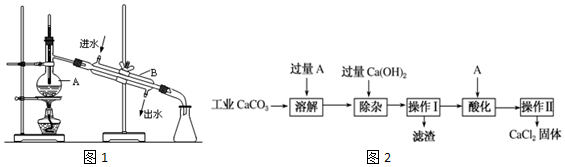
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 丙烯分子中3个碳原子都是sp3杂化 | |
| B. | 每个丙烯分子有7个σ键,1个π键 | |
| C. | 丙烯分子是存在非极性键和极性键的极性分子 | |
| D. | 丙烯分子为手性分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该溶液一定呈酸性 | B. | 该溶液中的c(H+)可能等于10-3 | ||
| C. | 该溶液的pH可能为2,可能为12 | D. | 该溶液有可能呈中性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 用图1装置制取并收集干燥纯净的NH3 | |
| B. | 用图2装置可演示NO的喷泉实验 | |
| C. | 用图3装置制备Fe(OH)2并能较长时间观察其颜色 | |
| D. | 用图4装置验证苯中是否有独立的碳碳双键 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
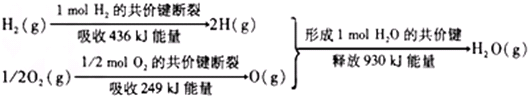
| A. | 氢气跟氧气反应生成水的同时释放能量 | |
| B. | 氢气跟氧气反应生成水的同时吸收能量 | |
| C. | 1 mol H2跟1/2 mol O2反应生成1 mol H2O释放能量不一定是245 kJ | |
| D. | 2 mol H2(g)跟1 mol O2(g)反应生成2 mol H2O(g)释放能量490 kJ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com