
| A、1:2 | B、1:1 |
| C、1:4 | D、2:1 |
| 54 |
| 102 |
| 14 |
| 17 |


 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案科目:高中化学 来源: 题型:
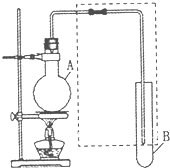 如图是用于简单有机化合物的制备、分离、性质比较等的常见简易装置.请
如图是用于简单有机化合物的制备、分离、性质比较等的常见简易装置.请查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1s22s22p63s23p63d54s1 |
| B、1s22s22p63s23p3 |
| C、1s22s22p63s23p63d64s2 |
| D、1s22s22p63s23p63d74s2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、IA族 | B、ⅡA族 |
| C、ⅢA族 | D、IVA族 |
查看答案和解析>>
科目:高中化学 来源: 题型:
+ 4 |
- 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、CaCO3
| ||||||||
B、Cu
| ||||||||
C、KMnO4
| ||||||||
D、NH3
|
查看答案和解析>>
科目:高中化学 来源: 题型:
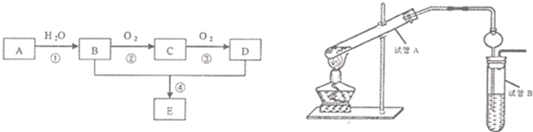
| 光照 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com