
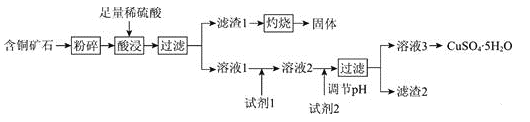
【题目】以某含铜矿石[主要成分为FeCu4SiO5(OH)4,含少量SiO2、CuCO3]为原料,制备CuSO4·5H2O的流程如下:
已知:
ⅰ.溶液中离子浓度小于等于1.0×10-5mol·L-1时,认为该离子沉淀完全。
ⅱ.相关试剂成分和价格如表1所示。
ⅲ.25℃时,该流程中金属离子生成氢氧化物时,开始沉淀和沉淀完全的pH如表2所示。
表1
试剂 | 成分 | 价格/(元·吨-1) |
漂白液 | 含25.2%NaClO | 450 |
双氧水 | 含30%H2O2 | 2400 |
浓硝酸 | 含98%HNO3 | 1500 |
表2
氢氧化物 | 开始沉淀的pH | 沉淀完全的pH |
Fe(OH)2 | 7.6 | 9.6 |
Fe(OH)3 | 2.7 | 3.7 |
Cu(OH)2 | 4.0 | 6.5 |
请回答:
(1)FeCu4SiO5(OH)4用氧化物的形式可表示为________。
(2)结合题中信息,所选用的试剂1的名称为________;加入该试剂时,所发生反应的离子方程式为________。
(3)加入试剂2,需调节溶液的pH的合理范围为________。试剂2可以选择下列物质中的________(填字母)。
A.Cu B.CuO
C.Cu(OH)2 D.Fe
(4)25℃时,Cu(OH)2的溶度积常数Ksp[Cu(OH)2]=________。
(5)CuSO4·5H2O溶液可用于电解精炼铜。电解精炼铜时,导线中通过9.632×104C的电量时,理论上阴极质量增加________g。(已知:1个电子的电量为1.6×10-19C)
【答案】 FeO·4CuO·SiO2·2H2O 漂白液 ClO-+2Fe2++2H+=Cl-+2Fe3++H2O 3.7≤pH<4.0 BC 1.0×10-20 32
【解析】试题分析:(1)FeCu4SiO5(OH)4用氧化物的形式表示时,先写活泼金属氧化物,再写不活泼金属氧化物,最后写非金属氧化物和水;(2)Cu2(OH)2CO3以及Fe、Si的化合物与稀硫酸反应生成硫酸铜、硫酸亚铁、硫酸铁。二氧化硅与稀硫酸不反应,所以滤液1中除含有Cu2+外,还含有的金属离子有Fe2+、Fe3+,为使溶液中铁元素沉淀析出,需要加氧化剂把Fe2+氧化为Fe3+,根据经济性、环境保护原则,选择漂白液做氧化剂;根据氧化还原反应规律配平方程式;(3)要让Fe3+完全沉淀,Cu2+不沉淀,根据金属离子生成氢氧化物时,开始沉淀和沉淀完全的pH表选择合适PH;选择试剂2,要依据不引入新杂质的原则;(4)根据铜离子浓度为1.0×10-5mol·L-1,溶液PH为6.5,计算25℃时,Cu(OH)2的溶度积常数Ksp[Cu(OH)2];(5)先根据电量计算电子的物质的量,再根据阴极反应![]() 计算生成铜的质量。
计算生成铜的质量。
解析:根据元素分析,(1)FeCu4SiO5(OH)4用氧化物的形式可表示为FeO·4CuO·SiO2·2H2O;(2)加入试剂1的目的是把Fe2+氧化为Fe3+,根据经济性、环境保护原则,选择漂液做氧化剂;反应离子方程式为ClO-+2Fe2++2H+=Cl-+2Fe3++H2O;(3)要让Fe3+完全沉淀, PH![]() 3.7,Cu2+不沉淀,PH<4.0,所以PH的合理范围为3.7≤pH<4.0;不引入新杂质,试剂2为CuO、Cu(OH)2;(4)Ksp[Cu(OH)2]= c(Cu2+)×c2(OH)2=1.0×10-5mol·L-1×(1.0×10-7.5 mol·L-1)2= 1.0×10-20;(5)电路中转移电子的物质的量为
3.7,Cu2+不沉淀,PH<4.0,所以PH的合理范围为3.7≤pH<4.0;不引入新杂质,试剂2为CuO、Cu(OH)2;(4)Ksp[Cu(OH)2]= c(Cu2+)×c2(OH)2=1.0×10-5mol·L-1×(1.0×10-7.5 mol·L-1)2= 1.0×10-20;(5)电路中转移电子的物质的量为![]() 1mol,根据
1mol,根据![]() ,生成铜的物质的量为0.5 mol,质量为32 g,理论上阴极质量增加32 g。
,生成铜的物质的量为0.5 mol,质量为32 g,理论上阴极质量增加32 g。


 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案科目:高中化学 来源: 题型:
【题目】一定温度下,在—定体积的密闭容器中,下列叙述能作为可逆反应A(S)+2B(g) ![]() C(g) +D (g)达到平衡状态标志的是
C(g) +D (g)达到平衡状态标志的是
A. 混合气题的平均分子量不再变化 B. 单位时间内消耗2a mol B,同时生成amol C
C. 2v正(B)=v逆(C) D. 混合气体的总压强不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表中的实线表示元素周期表的部分边界,a-j分别表示周期表中对应位置的元素。回答下列问题:

(1)请在上表中用实线补全元素周期表边界_______。
(2)元素b在元素周期表中的位置是_______;元素a与d形成的4核18电子物质的分子式_______。
(3)元素e、g、h的简单离子半径由小到大的顺序为______。(用离子符号表示)
(4)元素e的气态氢化物比元素i的气态氢化物稳定性______。(填“强”或“弱”)。
(5)元素d与f形成的化合物中,原子个数1:1的化合物所含化学键类型为 ______。
(6)用电子式表示元素i、j形成化合物的过程______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关金属铝及其化合物的叙述正确的是( )
A.铝在常温下不能与氧气反应
B.铝不能与氯气反应
C.氧化铝只能与酸反应,不能与碱反应
D.铝既能溶于酸,又能溶于强碱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质混合后不能发生离子反应的是( )
A. 硫酸溶液与食盐水 B. 硫酸铜溶液与氢氧化钠溶液
C. 锌片与稀硫酸 D. Cl2通入氢氧化钠溶液中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】糖类与我们的日常生活息息相关。关于糖类物质的说法正确的是
A. 糖类均有甜味 B. 淀粉和纤维素均不是糖类
C. 糖类均不可水解 D. 糖类都含有C、H和O元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 久置的漂白粉漂白效果更好
B. 以海水为原料能提取出Na、Mg、Br2等物质
C. 次氯酸和二氧化硫的漂白原理相同
D. 二氧化硅不与任何酸反应,可用石英制造耐酸容器
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com