

 Al2O3+2Fe,故答案为:2Al+Fe2O3
Al2O3+2Fe,故答案为:2Al+Fe2O3 Al2O3+2Fe;
Al2O3+2Fe;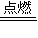 2[Al(OH)4]-+3H2↑,
2[Al(OH)4]-+3H2↑,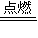 2[Al(OH)4]-+3H2↑;
2[Al(OH)4]-+3H2↑;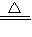 MnCl2+Cl2↑+2H2O,若有0.1molMnO2参加反应,生成Cl2气体的物质的量为0.1mol,体积是2.24L.
MnCl2+Cl2↑+2H2O,若有0.1molMnO2参加反应,生成Cl2气体的物质的量为0.1mol,体积是2.24L.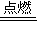 2MgO+C,
2MgO+C, 2MgO+C.
2MgO+C.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:

| ||
| ||
| ||
| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
| 1 |
| 2 |
| 3 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | 结构或性质信息 |
| T | 原子的L层上s电子数等于p电子数. |
| X | 元素的原子半径是第三周期主族元素中最大的. |
| Y | 空气中含其单质,原子的最外层未成对电子数是该元素所在周期中最多的. |
| Z | 单质常温、常压下是气体.原子的M层上有1个未成对的p电子. |

查看答案和解析>>
科目:高中化学 来源: 题型:
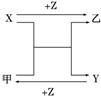 X、Y、Z是中学化学中三种常见元素的单质,甲、乙是两种常见的化合物,相互间有如图转化关系(未注明反应条件),下列说法不正确的是( )
X、Y、Z是中学化学中三种常见元素的单质,甲、乙是两种常见的化合物,相互间有如图转化关系(未注明反应条件),下列说法不正确的是( )| A、若X为金属单质,Y为非金属固体单质,则Z为O2 | B、若X、Y均为金属单质,则甲不可能为黑色固体 | C、若X为金属单质,Y为非金属气体单质,则乙可能为黑色固体 | D、若X、Y均为非金属固体单质,则Z可能为O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、X、Y、Z中,只有Y能使湿润的淀粉碘化钾试纸变蓝 | B、1mol Y或Z与足量水完全反应时,均转移2mol电子 | C、Z为离子化合物,但含有非极性键,阴、阳离子个数比为1:2 | D、X和Y均能用向上排空气法和排水法收集 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com