
| 物质 | Mg(OH)2 | CaCO3 | MgCO3 | Ca(OH)2 | CaSO4 | MgSO4 |
| $\frac{溶解度}{g/100g{H}_{2}O}$ | 9.0×10-4 | 1.5×10-3 | 1.0×10-2 | 1.7×10-1 | 2.1×10-1 | 26.7 |
分析 (1)在水中加热时Mg(HCO3)和MgCO3会转化为Mg(OH)2;
(2)CaSO4与酸不反应,必须先转化为碳酸钙,再加酸除去;
(3)根据自来水中的离子成分进行分析锅炉水垢中还可能含有的物质;
(4)根据Ca2+浓度求出其质量和物质的量,再根据M与Ca2+、Mg2+都以等物质的量进行反应,求算Mg2+的物质的量及浓度.
解答 解:(1)Mg(OH)2溶解度小于MgCO3,在加热时,MgCO3易转化生成Mg(OH)2,通过质量守恒定律可推测出反应方程式:Mg(HCO3)2$\frac{\underline{\;\;△\;\;}}{\;}$MgCO3↓+H2O+CO2↑,MgCO3+H2O$\frac{\underline{\;\;△\;\;}}{\;}$ Mg(OH)2+CO2↑
故答案为:Mg(HCO3)2$\frac{\underline{\;\;△\;\;}}{\;}$MgCO3↓+H2O+CO2↑,MgCO3+H2O$\frac{\underline{\;\;△\;\;}}{\;}$ Mg(OH)2+CO2↑;
(2)CaSO4与酸不反应,必须先转化为碳酸钙,再加酸除去,所以要先加入碳酸钠;CaSO4能转化为物质碳酸钙的原因是碳酸钙的溶解度小于硫酸钙的溶解度,
故答案为:C;碳酸钙的溶解度小于硫酸钙的溶解度;
(3)由于自来水中含有Ca2+、Mg2+、Na+、K+、HCO3-、SO42-、Cl-,所以加热过程中会生成CaSO4、Mg(OH)2、MgCO3和CaCO3,
故答案为:MgCO3和CaCO3;
(4)10mL自来水样中Ca2+的质量为0.40g/L×10×10-3L=4×10-3g,则n(Ca2+)=$\frac{m}{M}$=$\frac{4×1{0}^{-3}g}{40g/mol}$=1×10-4mol,
已知M与Ca2+、Mg2+都以等物质的量进行反应,所以n(Ca2+)=n(M)-n(Ca2+)=0.01mol/L×20×10-3L-1×10-4mol=1×10-4mol,
所以c(Mg2+)=$\frac{n}{V}$=$\frac{1×1{0}^{-4}mol}{10×1{0}^{-3}L}$=0.01mol/L;
故答案为:0.01mol/L.
点评 本题考查物质分离和提纯,为高频考点,涉及离子浓度的求算、新信息处理能力及书写化学方程式的能力,正确把握信息的获取和解答是解本题关键,题目难度不大.


 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:选择题
| A. | $\frac{n(A-N+8)}{A+16}$ | B. | $\frac{n(A-N+10)}{(A+16)}$ | C. | A-N+2 | D. | $\frac{n(A-N+6)}{A}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
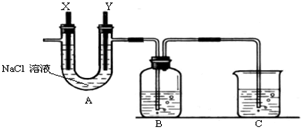
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 “白铁皮”具有较强的耐腐蚀性,是生产中常用的金属材料之一.镀锌层犹如铁皮的保护层,这层膜的厚度及均匀度也成了判断镀层质量的重要指标.某研究性学习小组为了测定镀锌铁皮的厚度,设计了下面的实验方案:
“白铁皮”具有较强的耐腐蚀性,是生产中常用的金属材料之一.镀锌层犹如铁皮的保护层,这层膜的厚度及均匀度也成了判断镀层质量的重要指标.某研究性学习小组为了测定镀锌铁皮的厚度,设计了下面的实验方案:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | MgCl2(熔融)$\frac{\underline{\;电解\;}}{\;}$Mg+Cl2↑ | B. | Al2O3+3H2$\frac{\underline{\;\;△\;\;}}{\;}$2Al+3H2O | ||
| C. | Fe3O4+4CO$\frac{\underline{\;\;△\;\;}}{\;}$3Fe+4CO2 | D. | 2HgO$\frac{\underline{\;\;△\;\;}}{\;}$2Hg+O2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com