
 在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系.下列条件关于离子共存说法中正确的是( )
在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系.下列条件关于离子共存说法中正确的是( )| A. | a点对应的溶液中大量存在:Fe3+、Na+、SO42-、Cl- | |
| B. | b点对应的溶液中大量存在:Fe2+、Cl-、NO3-、Na+ | |
| C. | c点对应的溶液中大量存在:Ba2+、Cl-、Na+、Br- | |
| D. | d点对应的溶液中大量存在:Cu2+、K+、SO42-、NO3- |
分析 水的离子积为Kw=c(H+)×c(OH-),由图可知,a、b均在25℃,离子积相同;而c、d均在T℃,离子积相同,并结合离子之间不发生化学反应来解答.
解答 解:A.Fe3+水解显酸性,而a点对应的溶液显中性,则离子不能大量共存,故A错误;
B.b点溶液呈酸性,Fe2+、NO3-发生氧化还原反应,故B错误;
C.c点对应的溶液显中性,离子之间不发生任何反应,可大量共存,故C正确;
D.d点时c(H+)<c(OH-),溶液碱性,Cu2+不能大量共存,故D错误.
故选C.
点评 本题考查离子的共存,明确图象中各点对应的溶液的酸碱性是解答本题的关键,注意T℃>25℃为学生解答的难点,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 推广垃圾分类存放,分类回收,分类处理 | |
| B. | 改革传统采煤时将煤层气(瓦斯气,主要成分甲烷)直接排入空气的做法,采用先开采和综合利用煤层气,然后再采煤的方法 | |
| C. | 推荐使用手帕,尽量减少使用面纸 | |
| D. | 将工厂的烟囱造高,以减少工厂周围的大气污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用铁作阳极,电解饱和食盐水的离子方程式:Fe+2H2O$\frac{\underline{\;电解\;}}{\;}$Fe(OH)2↓+H2↑ | |
| B. | 溴乙烷的消去反应:CH3CH2Br$→_{△}^{浓硫酸}$ CH2=CH2↑+HBr | |
| C. | CH4燃烧热的热化学方程式:CH4(g)+2O2(g)═CO2(g)+2H2O(g) H=-802.3 kJ•mol-1 | |
| D. | 示踪原子法研究乙酸与乙醇酯化反应: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钠用于治疗胃溃疡病人的胃酸过多症 | |
| B. | 在AlCl3溶液中加入过量氨水最终无沉淀生成 | |
| C. | 工业上可利用钠和TiCl4溶液反应制取金属Ti | |
| D. | 锅炉中水垢可用盐酸或醋酸除去 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学平衡常数的大小与温度、浓度、压强有关,与催化剂无关 | |
| B. | 已知:K1 (H2CO3)>Ka (HClO)>K2(H2CO3),向NaClO溶液中通入少量CO2的化学方程是:2NaClO+CO2+H2O=Na2CO3+2HClO | |
| C. | 25℃时,pH=4的盐酸中,KW=10-20 | |
| D. | 常温下,Ksp(CaSO4)=9×10-6,向100mL饱和CaSO4溶液中加400mL 0.01mol/LNa2SO4溶液,无沉淀析出 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
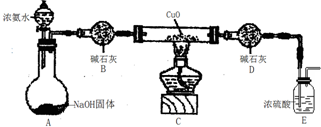
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金刚石的网状结构中,以共价键形成的最小碳环上有6个碳原子 | |
| B. | 氯化铯晶体中,每个Cs+周围紧邻8个Cl- | |
| C. | 氯化钠晶体中,每个Na+周围距离最近且相等的Na+共有6个 | |
| D. | 石墨晶体中,每一层内碳原子数与碳碳键数之比为2:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
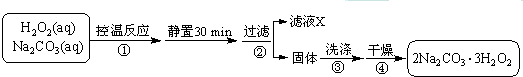
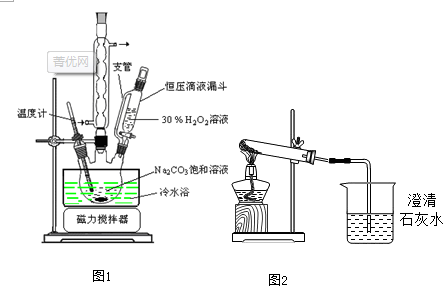
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com