
【题目】三苯甲醇是有机合成中间体。实验室用格式试剂(![]() )与二苯酮反应制备三苯甲醇。
)与二苯酮反应制备三苯甲醇。
已知:①格式试剂非常活泼,易与水反应
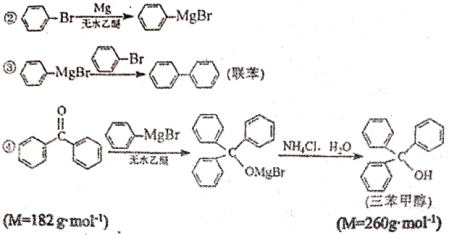
实验过程如下:
①合成格氏试剂:实验装置如图1所示,向三颈烧瓶加入0.75g镁屑和1小粒碘,装好装置,在恒压漏斗中加入3.20 mL溴苯(0.03 mol)和15.00 mL乙醚混匀,开始缓慢滴入三颈烧瓶,滴完后待用。
②制备三苯甲醇:实验装置如图1所示,将5.5g二苯酮与15 mL乙醇在恒压漏斗中混匀,滴入三颈烧瓶。40℃左右水浴回流0.5h,加入20mL饱和氯化铵溶液,使晶体析出,经过系列操作得到粗产品。
③提纯:用图2所示装置进行提纯,最后冷却抽滤.
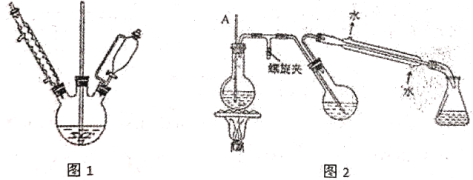
(1)实验中乙醚溶剂必须预先用_______试剂除去溶解在其中痕量的水,再经过_______得到;
A 浓硫酸 B 金属钠 C 过滤 D 蒸馏
(2)图1实验中,实验装置存在缺陷,应在球形冷凝管上连接_________装置;
(3)合成格氏试剂过程中,如果混合液滴加过快将导致格氏试剂产率下降,其原因是_______;
(4)在制备三苯甲醇的过程中,不能先将20mL饱和氯化铵溶液一起加入后再水浴回流的原因是__________;
(5)步骤②中系列操作为_________、过滤、洗涤、_________;
A 蒸发结晶 B 冷却结晶 C 高温烘干 D 滤纸吸干
(6)下列关于减压过滤的操作或说法正确的是________
A 滤纸大小适当,盖满所有孔,用溶剂润湿滤纸,微开水龙头,抽气使滤纸紧贴漏斗瓷板上
B 不宜过滤胶状沉淀,因为胶状沉淀颗粒太小易在滤纸上形成一层密实的沉淀
C 减压过滤完毕,先关闭水龙头,后拆下连接抽气泵和吸滤瓶的橡皮管,防止倒吸
D 实验过程要注意吸滤瓶内液面高度,当快到达支管口位置时,应先拔掉吸滤瓶上的橡皮管,再从支管口倒出滤液
E 当过滤的溶液具有强酸性、强氧化性时,可用玻璃纤维代替滤纸或用玻璃砂漏斗代替布氏漏斗
(7)通过提纯得到产品4.00g,则本实验产率为_________(计算结果保留3位有效数字)
【答案】B C 干燥 滴加过快导致生成的格氏试剂与溴苯反应生成副产物联苯,导致格氏试剂产率下降 先将20ml饱和氯化铵溶液一起加入会导致格氏试剂与水反应,使三苯甲醇产率降低 B D A E 0.513
【解析】
(1)乙醚中含有极少量水时通常用金属钠干燥,然后经过过滤得到无水乙醚;
(2)考虑格林试剂易与水反应;
(3)滴入过快会产生联苯,使格林试剂产率下降;
(4)格式试剂非常活波,易与水反应,加入饱和氯化铵溶液会发生反应导致三苯甲醇产率减小;
(5)冷却结晶、过滤、洗涤、滤纸吸干得到晶体;
(6)根据减压过滤的操作进行分析;
(7) 0.03mol溴苯理论上得到0.03mol格林试剂,则理论上得到三苯甲醇0.03mol,即理论上生成的三苯甲醇的质量为0.03mol×260g/mol=7.80g,据此计算可得。
(1)乙醚中含有极少量水时通常用金属钠干燥,然后经过过滤得到无水乙醚;故答案为:B;C;
(2)已知格氏试剂非常活泼,易与水反应,故在制备格林试剂中为防止格林试剂变质,应在球形冷凝管上连接干燥装置;故答案为:干燥;
(3)根据题目信息,滴入过快会产生联苯,使格林试剂产率下降,故合成格氏试剂过程中,缓慢滴加混合液;故答案为:滴加过快导致生成的格氏试剂与溴苯反应生成副产物联苯,导致格氏试剂产率下降;
(4)格式试剂非常活波,易与水反应,加入饱和氯化铵溶液会发生反应导致三苯甲醇产率减小;故答案为:先将20ml饱和氯化铵溶液一起加入会导致格氏试剂与水反应,使三苯甲醇产率降低;
(5)反应结束后,反应液冷却结晶、过滤、洗涤、滤纸吸干可得到三苯甲醇晶体;故答案为:B;D;
(6)A.滤纸略小于布氏漏斗,但要把所有的孔都覆盖,并用蒸馏水润湿滤纸,微开水龙头,抽气使滤纸紧贴在漏斗瓷板上,故A正确;
B.抽滤不宜用于过滤胶状沉淀,因为胶状颗粒容易透过滤纸,故B错误;
C.由于装置中存在压强差,所以抽滤结束后,应先拆下连接抽气泵和吸滤瓶的橡皮管,后关闭水龙头,故C错误;
D.注意吸滤瓶内液面高度,当吸滤瓶中液面快达到支管口位置时,应拔掉吸滤瓶上的橡皮管,从吸滤瓶上口倒出溶液,故D错误;
E.当过滤的溶液具有强酸性、强氧化性时,可能会与滤纸发生反应,可用玻璃纤维代替滤纸或用玻璃砂漏斗代替布氏漏斗,故E正确;
故答案为:AE;
(7)0.03mol溴苯理论上得到0.03mol格林试剂,则理论上得到三苯甲醇0.03mol,即理论上生成的三苯甲醇的质量为0.03mol×260g/mol=7.80g,故产率为:![]() ×100%=0.513;故答案为:0.513。
×100%=0.513;故答案为:0.513。


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
【题目】常温下,下列叙述正确的是( )
A. 盐酸溶液的导电能力一定比醋酸溶液的强
B. 在滴有酚酞溶液的氨水中,加入NH4Cl的溶液恰好无色,则此时溶液的pH< 7
C. 向10 mL 0.1 mol·L-1的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中,![]() 将减小
将减小
D. 用已知浓度的NaOH溶液滴定未知浓度的醋酸溶液,最好选用甲基橙作指示剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一包铝热剂(铝粉和氧化铁的混合物),进行如下实验,①向一份铝热剂中加入800ml 2mol/L的氢氧化钠溶液,使其充分反应后,收集到的气体体积为20.16L(S.T.P.)②另一份等质量的铝热剂在高温下充分反应后,向反应后固体中加入2L 2.5mol/L的盐酸溶液,使固体完全溶解,反应后溶液PH=0(假设过程中溶液体积不变),取少量反应后溶液,滴加硫氰化钾,没有出现血红色.完成下列计算:
(1)计算该铝热剂中铝与氧化铁物质的量之比?_______________
(2)实验②产生的气体的体积是多少?(S.T.P.)______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.2,2-二甲基丁烷的1H-NMR上有4个峰
B.![]() 中所有原子处于同一平面上
中所有原子处于同一平面上
C.一定条件下1 mol![]() 与KOH溶液反应,最多消耗3 mol的KOH
与KOH溶液反应,最多消耗3 mol的KOH
D.甲苯能使酸性KMnO4溶液褪色,说明苯环与甲基相连的碳碳单键变活泼,被KMnO4氧化而断裂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】侯氏制碱法原理是:NH3+H2O+CO2+NaCl=NaHCO3↓+NH4Cl析出碳酸氢钠,下列实验装置及原理设计说法不合理的是:
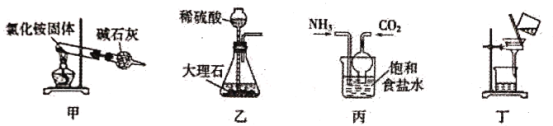
A.用装置甲制取氨气时得到氨气很少,主要原因是分解得到NH3、HCl的遇冷会重新化合
B.用装置乙生成的CO2速率很慢,原因是反应生成微溶于水的硫酸钙,覆盖着大理石的表面
C.用装置丙模拟侯氏制碱法,可以同时通入NH3、CO2,也可以先通氨气再通CO2
D.用装置丁分离得到产品NaHCO3,为得到干燥产品,也可采用减压过滤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20mL0.1mol/L NaHA(酸式盐)溶液中分别滴加0.1mol/L 盐酸或0.1mol/L NaOH溶液,溶液的pH与滴加溶液体积关系如图所示。下列推断正确的是( )
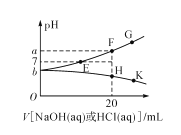
A.NaHA在水中电离程度大于水解程度
B.在对应的各点溶液中,H点水电离程度最大
C.E点对应的溶液中有c(Na+)=c(HA-)+c(A2-)
D.F点对应的溶液中存在c(H+)+c(Na+)=(OH-)+c(HA-)+c(A2-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭体系中发生下列反应:N2(g)+3H2(g)![]() 2NH3(g)△H<0,如图所示是某一时间段中反应速率与反应进程的曲线关系图,回答下列问题:
2NH3(g)△H<0,如图所示是某一时间段中反应速率与反应进程的曲线关系图,回答下列问题:

(1)处于平衡状态的时间段是__.
(2)t1、t3、t4时刻体系中分别改变的是什么条件?
t1:__,t3:__,t4:__.
(3)下列各时间段时,氨的体积分数最高的是______。
A.t2~t3 B.t3~t4 C.t4~t5 D.t5~t6.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配制100 mL 1.0 mol/LNa2CO3溶液,下列操作正确的是
A. 称取10.6 g无水碳酸钠,加入100 mL容量瓶中,加水溶解、定容
B. 称取10.6 g无水碳酸钠,加入100 mL蒸馏水,搅拌、溶解
C. 转移Na2CO3溶液时,未用玻璃棒引流,直接倒入容量瓶中
D. 定容后,塞好瓶塞,反复倒转、摇匀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两份质量相等的Na2O2和NaHCO3混合物,其中一份加入足量的盐酸充分反应后放出2.24L(标准状况)的气体;将这些气体通入另一份混合物中使其充分反应,气体体积变为2.016L(标准状况).则原混合物中Na2O2和NaHCO3的物质的量之比为
A.8:1B.2:1C.3:2D.2:9
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com