


科目:高中化学 来源: 题型:
| A、化学将在能源、资源的合理开发和安全应用方面大显身手 |
| B、化学面对现代日益严重的环境问题显得无能为力 |
| C、化学是一门具有极强实用性的科学 |
| D、化学是一门以实验为基础的自然科学 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、混合物:空气、矿泉水、水银 |
| B、碱:Ba(OH)2、纯碱、NH3?H2O |
| C、盐:石灰石、氯化铵、NaHSO4 |
| D、酸性氧化物:CO2、CO、SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
2- 4 |
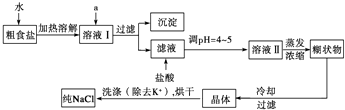
2- 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 2010上海世博上,零排放、太阳能、绿色光源等成为高科技亮点.
2010上海世博上,零排放、太阳能、绿色光源等成为高科技亮点.查看答案和解析>>
科目:高中化学 来源: 题型:
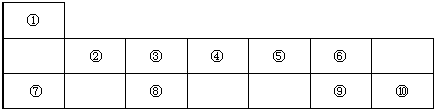
| X | Y | Z |
| 甲 | 乙 | 丙 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com