
分析 (1)Mg与二氧化碳反应生成MgO和C;
(2)Cu与氯化铁反应生成氯化亚铁、氯化铜;
(3)钠为活泼金属,容易与水分反应生成具有腐蚀性的氢氧化钠;
(4)CO还原氧化铁生成Fe、二氧化碳;
(5)氯气与石灰乳反应生成氯化钙和次氯酸钙,漂白粉的有效成分为次氯酸钙,结合反应的方程式计算;
(6)Fe2+氧化成Fe3+,可以选择氧化剂氯水,氯气氧化亚铁离子为三价铁离子,检验铁离子用硫氰酸钾溶液检验,硫氰酸根离子和铁离子反应生成血红色溶液,证明铁离子的存在;
(7)Cu与浓硫酸加热生成硫酸铜、二氧化硫和水.
解答 解:(1)镁燃烧时不能用二氧化碳来扑灭,其原因是Mg能与二氧化碳反应,故答案为:Mg能与二氧化碳反应;
(2)Cu与氯化铁反应生成氯化亚铁、氯化铜,离子反应为2Fe3++Cu=2Fe2++Cu2+,故答案为:2Fe3++Cu=2Fe2++Cu2+;
(3)金属钠性质非常活泼,能够与手上的水分反应生成氢氧化钠,腐蚀皮肤,所以不能用手直接拿取金属钠,
故答案为:金属钠会和手上的水分反应生成氢氧化钠,腐蚀皮肤;
(5)氯气与Ca(OH)2反应生成CaCl2、Ca(ClO)2和水,反应的方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,漂白粉的有效成分为次氯酸钙,在反应中,氯气既是氧化剂又是还原剂,由方程式可知氧化剂与还原剂物质的量之比是1:1,
故答案为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;Ca(ClO)2;1:1;
(6)Fe2+氧化成Fe3+,可以选择氧化剂氯水,氯气氧化亚铁离子为三价铁离子,反应的离子方程式为:2Fe2++Cl2=2Fe3++2Cl-;检验铁离子用硫氰酸钾溶液检验,硫氰酸根离子和铁离子反应生成血红色溶液,证明铁离子的存在;
故答案为:2Fe2++Cl2=2Fe3++2Cl-;KSCN;溶液变为红色;
(7)Cu与浓硫酸加热生成硫酸铜、二氧化硫和水,反应为Cu+2H2SO4(浓) $\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O,故答案为:Cu+2H2SO4(浓) $\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O.
点评 本题考查金属及化合物的性质,为高频考点,把握常见金属的性质、发生的反应为解答的关键,注重基础知识的夯实,侧重分析与应用能力的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 碱金属单质的密度都比水小 | |
| B. | 碱金属单质都是还原剂 | |
| C. | 碱金属单质的熔沸点一般随着原子的电子层数的增多而升高 | |
| D. | 碱金属单质在氧气中燃烧,产物都是过氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
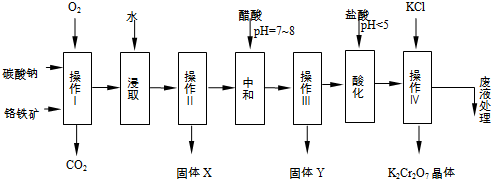
| 物质 | 溶解度/(g/100g水) | ||
| 0°C | 40°C | 80°C | |
| KCl | 28 | 40.1 | 51.3 |
| NaCl | 35.7 | 36.4 | 38 |
| K2Cr2O7 | 4.7 | 26.3 | 73 |
| Na2Cr2O7 | 163 | 215 | 376 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 新制氯水只含Cl2和H2O两种分子 | B. | 氢氟酸不能贮放在玻璃瓶里 | ||
| C. | 光导纤维的主要成分是二氧化硅 | D. | 浓硫酸用铁制容器密封保存 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向某无色溶液中加入BaCl2,产生白色浑浊说明该溶液中一定有SO42- | |
| B. | 向淀粉碘化钾溶液中加氯水,溶液变为蓝色说明氯气的氧化性强于碘单质 | |
| C. | 硫酸能与NaCl反应生成HCl,说明硫酸的酸性比盐酸强 | |
| D. | 向某溶液中滴加稀盐酸无明显现象,再加硝酸银产生白色沉淀,说明溶液中含Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁与稀盐酸反应 2Fe+6H+═2Fe3++3H2↑ | |
| B. | 硝酸银溶液中加入铜粉 Ag++Cu═Cu2++Ag | |
| C. | 氧化铜与盐酸反应 O2-+2H+═H2O | |
| D. | 碳酸镁跟稀硫酸反应:MgCO3+2H+═Mg2++H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | CuSO4[Cu(OH)2] | B. | NaOH[NaOH] | C. | CuCl2[CuCl2] | D. | NaCl[NaCl] |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6.4 g | B. | 4.8 g | C. | 2.4 g | D. | 1.6 g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com