
向体积为2 L的密闭容器中充入2 mol SO2和1 mol O2,测得起始容器压强为p,一定条件下发生反应:2SO2(g)+O2(g) 2SO3(g) △H=-196 kJ·mol-1,维持容器温度不变,测得平衡时容器内压强为0.7p,若此时再向容器中充入2 mol SO3,则下列说法正确的是
2SO3(g) △H=-196 kJ·mol-1,维持容器温度不变,测得平衡时容器内压强为0.7p,若此时再向容器中充入2 mol SO3,则下列说法正确的是
| A.充入2 mol SO3后,SO2的物质的量增大 |
| B.第一次反应达到平衡时共放出热量176.4 kJ |
| C.充入2 mol SO3达到新平衡时,容器内的压强为1.4p |
| D.降低容器的温度可使新平衡时各物质的体积分数与第一次平衡时相同 |
科目:高中化学 来源: 题型:
能源短缺是人类社会面临的重大问题。甲醇是一种可再生能源,具有广泛的开发和应用前景。
(1)工业上一般采用下列两种反应合成甲醇:
反应I:CO(g) + 2H2(g) ![]() CH3OH(g) ΔH1
CH3OH(g) ΔH1
反应II: CO2(g) + 3H2(g) ![]() CH3OH(g) + H2O(g) ΔH2
CH3OH(g) + H2O(g) ΔH2
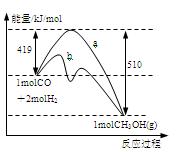
右图是反应I反应过程中的能量变化曲线。
(1)由右图可知反应I为 反应(选填”吸热、放热”),反应热△H1=
(2)反应I在一定体积的密闭容器中进行,能判断其是否达到化学平衡状态的依据是 。
A.容器中压强不变 B.混合气体中c(CO)不变
C.v正(H2)=v逆(CH3OH) D.c(CO)=c(CH3OH)
(3)图中曲线 表示使用催化剂时反应的能量变化。
(4)一定条件下,向体积为2 L的密闭容器中充入2 mol CO2和6 mol H2,一段时间后达到平衡状态,测得CH3OH(g)的物质的量为1mol,则此条件下该反应的化学平衡常数数
K值= (用分数表示),若开始时充入2 mol CH3OH(g) 和2 mol H2O(g)达到相同平衡时CH3OH的转化率为 ,若平衡后在充入4 mol的N2,则C(CO2)是 。
(5)从绿色化学的角度比较上述两种方法,符合原子经济的是 。(填“I” 或“II”)
查看答案和解析>>
科目:高中化学 来源:2013-2014学年甘肃省武威市高三上学期第五次月考化学试卷(解析版) 题型:选择题
已知:CO2(g) + 3H2(g)  CH3OH(g)
+ H2O(g) ΔH=-49.0 kJ•mol-1。一定条件下,向体积为2 L的密闭容器中充入2 mol
CO2和6 mol H2,测得CO2和CH3OH(g)的浓度随时间变化曲线如图所示。下列叙述中,正确的是
CH3OH(g)
+ H2O(g) ΔH=-49.0 kJ•mol-1。一定条件下,向体积为2 L的密闭容器中充入2 mol
CO2和6 mol H2,测得CO2和CH3OH(g)的浓度随时间变化曲线如图所示。下列叙述中,正确的是

A.10min后,升高温度能使 增大
增大
B.反应达到平衡状态时,CO2的平衡转化率为75%
C.3 min时,用CO2的浓度表示的正反应速率等于用CH3OH的浓度表示的逆反应速率
D.从反应开始到平衡,H2的平均反应速率υ(H2)=0.075 mol·L-1•min-1
查看答案和解析>>
科目:高中化学 来源:2011-2012学年江苏省、大丰高中、栟茶高中高三第二次调研联考化学试卷 题型:选择题
向体积为2 L的密闭容器中充入2 mol
SO2和1 mol O2,测得起始容器压强为p,一定条件下发生反应:2SO2(g)+O2(g) 2SO3(g)
△H=-196 kJ·mol-1,维持容器温度不变,测得平衡时容器内压强为0.7p,若此时再向容器中充入2 mol SO3,则下列说法正确的是
2SO3(g)
△H=-196 kJ·mol-1,维持容器温度不变,测得平衡时容器内压强为0.7p,若此时再向容器中充入2 mol SO3,则下列说法正确的是
A.充入2 mol SO3后,SO2的物质的量增大
B.第一次反应达到平衡时共放出热量176.4 kJ
C.充入2 mol SO3达到新平衡时,容器内的压强为1.4p
D.降低容器的温度可使新平衡时各物质的体积分数与第一次平衡时相同
查看答案和解析>>
科目:高中化学 来源:2011-2012学年江苏省高三第二次调研联考化学试卷 题型:选择题
向体积为2 L的密闭容器中充入2 mol SO2和1 mol O2,测得起始容器压强为p,一定条件下发生反应:2SO2(g)+O2(g)  2SO3(g) △H=-196 kJ·mol-1,维持容器温度不变,测得平衡时容器内压强为0.7p,若此时再向容器中充入2 mol SO3,则下列说法正确的是
2SO3(g) △H=-196 kJ·mol-1,维持容器温度不变,测得平衡时容器内压强为0.7p,若此时再向容器中充入2 mol SO3,则下列说法正确的是
A.充入2 mol SO3后,SO2的物质的量增大
B.第一次反应达到平衡时共放出热量176.4 kJ
C.充入2 mol SO3达到新平衡时,容器内的压强为1.4p
D.降低容器的温度可使新平衡时各物质的体积分数与第一次平衡时相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com