
| ��ѧʽ | ����ƽ�ⳣ����25�棩 |
| HCN | K=4.9��10-10 |
| CH3COOH | K=1.8��10-5 |
| H2CO3 | K1=4.3��10-7��K2=5.6��10-11 |
���� ��1����ĵ��볣����������жϣ�Խ��������Ӧ��ˮ��̶�ԽС��
��2����Һ�е���غ���������
��3�����볣����С������Ӧ���ɲ������ƽ�ⳣ���ȽϿ�֪���ԣ�H2CO3��HCN��HCO3-�����Է�Ӧ���������̼�����ƣ���
��4���������Һ�е���غ���㣬PH=8��Һ�Լ��ԣ�
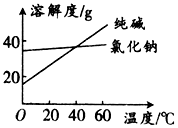
��� �⣺��1������ͼ�����ݷ�����������볣�������������̼��������ӣ����Ե�Ũ�ȵ�NaCN��Һ��Na2CO3��Һ��CH3COONa��Һˮ��̶ȵ�Ũ�ȵ�Na2CO3��Һ��NaCN��Һ��CH3COONa��Һ����ҺpHΪNa2CO3��Һ�ģ�NaCN��Һ�ģ�CH3COONa��Һ�ģ�
�ʴ�Ϊ��Na2CO3��Һ��NaCN��Һ��CH3COONa��Һ��
��2����Ũ�ȵ�CH3COOH��Һ��NaOH��Һ�������ϣ�������Һ�Լ��ԣ�c��H+����c��OH-��������Һ�е���غ�c��H+��+c��Na+��=c��OH-��+c��CH3COO-����c��Na+����c��CH3COO-����
�ʴ�Ϊ������
��3����NaCN��Һ��ͨ������CO2 ��H2CO3���Դ���HCN����HCO3-�����Է�Ӧ���������̼�����ƣ��������ɶ�����̼����Ӧ�Ļ�ѧ����ʽΪ��NaCN+H2O+CO2=HCN+NaHCO3��
�ʴ�Ϊ��NaCN+H2O+CO2=HCN+NaHCO3��
��4��25��ʱ��pH=8��CH3COONa��Һ�У�c��H+��=10-8mol/L��c��OH-��=$\frac{1{0}^{-14}}{1{0}^{-8}}$=10-6mol/L����Һ�д��ڵ���غ㣺c��Na+��+c��H+��=c��CH3COO-��+c��OH-��
c��Na+��-c��CH3COO-��=c��OH-��-c��H+��=10-6mol/L-10-8mol/L=9.9��10-7 mol/L��
�ʴ�Ϊ��9.9��10-7 mol/L��
���� ���⿼����������ʵ���ƽ��ķ����жϡ�����ˮ��Ӧ�á���Һ����Եļ��㡢���ӻ����������жϣ�ע��̼���Ƕ�Ԫ����ֲ����룬�ڶ��������ƽ�ⳣ��������С����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | c��Fe3+��=0.1 mol/L��Һ�У�Na+��NH4+��SCN-��SO42- | |
| B�� | ���ܽ�CaCO3����Һ�У�Fe3+��Ca2+��Cl-��NO3- | |
| C�� | ��ˮ�������c��H+��=1��10-2mol/L����Һ�У�Na+��Ba2+��HCO3-��Cl- | |
| D�� | ǿ������Һ�У�K+��Na+��ClO-��I- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | O2�������� | B�� | NH3�������� | C�� | O2����ԭ | D�� | NH3����������Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �Ķ��������в��ϣ�
�Ķ��������в��ϣ�| ���� | �۵�/�� | �е�/�� | �ܶ�/g•cm-3 | �ܽ��� |
| �Ҷ��� C2H6O2 | -11.5 | 198 | 1.11 | ������ˮ���Ҵ��������л��ܼ� |
| ������ C3H8O3 | 17.9 | 290 | 1.26 | �ܸ�ˮ�;ƾ�������Ȼ��ܣ������������л��ܼ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��һ��������ܱ������У����з�Ӧ��CO2��g��+H2��g��?CO��g��+H2O��g�����䷴Ӧ��ѧƽ�ⳣ����T�Ĺ�ϵ�����ʾ��
��һ��������ܱ������У����з�Ӧ��CO2��g��+H2��g��?CO��g��+H2O��g�����䷴Ӧ��ѧƽ�ⳣ����T�Ĺ�ϵ�����ʾ��| T/�� | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com