
【题目】在反应mA+nB===pC+qD中,若v(A)=4 mol·L-1·min-1, 而v(B)=1 mol·L-1·min-1,A表示的反应速率比B表示的反应速率快,而m、n符合的关系
A. m∶n=4∶1 B. m∶n<4∶1 C. m∶n>4∶1 D. 无法判断
科目:高中化学 来源: 题型:
【题目】在不同温度下,水溶液中c(H+)与c(OH-)关系如图所示。下列说法不正确的是 ( )
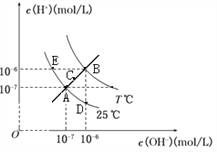
A. 图中五点Kw间的关系:B>C>A=D=E
B. 若从A点到C点,可采用温度不变在水中加入适量NH4Cl的方法
C. E点对应的水溶液中,可能有NH4+、Ba2+、Cl-、I-大量同时存在
D. 若处在B点时,将pH =2的硫酸溶液与pH = 10的KOH溶液等体积混合,所得溶液呈中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】PbCrO4是一种黄色颜料,制备PbCrO4的一种实验步骤如下:
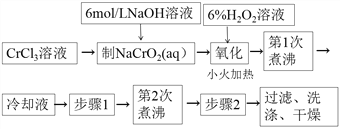
除图中标注的试剂外,实验中还用到6mol·L-1 醋酸,0.5 mol·L-1 Pb(NO3)2溶液,pH 试纸。
已知:①部分物质性质如下
物质 | 性质 | 颜色 | 溶解性 |
Cr(OH)3 | 两性氢氧化物 | 绿色 | 难溶于水 |
Pb(NO3)2 | - | 无色 | 易溶于水 |
Pb(CH3COO)2 | - | 无色 | 易溶于水 |
PbCrO4 | - | 黄色 | 难溶于水 |
Pb(OH)2 | 弱碱性 | 白色 | PH=7.2开始沉淀 ;PH=8.7完全沉淀 |
②PbCrO4可由沸腾的铬酸盐溶液与铅盐溶液作用制得,含PbCrO4晶种时更易生成
③六价铬在溶液中物种分布分数与pH关系如下图所示。
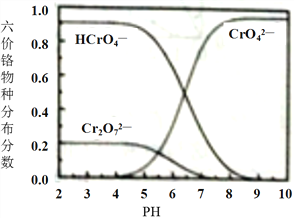
(1)“制NaCrO2(aq)”时,控制NaOH溶液加入量的操作方法是______。
(2)“氧化”时发生反应的离子方程式为______。
(3)下列说法正确的是(______)
A.两次煮沸的目的不相同
B.步骤2可以先加入一滴0.5mol·LPb(NO3)2溶液搅拌片刻,待产生少量沉淀后,继续滴加至有大量沉淀产生。
C.静置后,向上层清液中继续滴入Pb(NO3)2溶液,若无沉淀生成,则说明滴加完全。
D.小火加热的目的是为了避免反应过快。
(4)步骤1为__________________________________________________________。
(5)为测定产品的纯度,可用先用硝酸溶解PbCrO4,然后用EDTA(简写为Y4-)标准溶液滴定,反应的离子方程式:Pb2+ + Y4- =PbY2-。测定时,先称取0.5000g无水PbCrO4产品,溶解后,用0.05000 mol·L-1的EDTA标准溶液滴定至终点,消耗EDTA标准溶液26.50 mL,则测得无水PbCrO4产品的纯度是_________(以质量分数表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】游离态碳在自然界存在形式有多种,在工业上有着重要用途。请回答下列问题:
(1)我国四大发明之一的黑火药由木炭与硫黄、硝酸钾按一定比例混合而成。黑火药爆炸时生成硫化钾、氮气和二氧化碳。其爆炸的化学方程式为_____________________________________。
(2)高级碳粉可由烃类高温分解而制得,已知几个反应的热化学方程式:
C(s)+O2(g)==CO2(g) △H1= -393.5 kJmol-1
2H2(g)+O2(g)=2H2O(1) △H2= -571.6 kJmol-1
CH4(g)+2O2(g)-=CO2(g)+ 2H2O(1) △H3= -890.3 kJmol-1
则由天然气生产高级碳粉的热化学方程式为__________________________________。
(3)活性炭可以用来净化气体和液体。
①用活性炭还原氮氧化物,可防止空气污染。向1L闭容器加入一定量的活性炭和NO,某温度下发生反应C(s)+2NO(g)![]() N2(g)+CO2(g),测得不同时间内各物质的物质的量如下表:
N2(g)+CO2(g),测得不同时间内各物质的物质的量如下表:
物质的量/mol 时间/min | NO | N2 | CO2 |
0 | 0.200 | 0 | 0 |
10 | 0.116 | 0.042 | 0.042 |
20 | 0.080 | 0.060 | 0.060 |
30 | 0.080 | 0.060 | 0.060 |
此温度下,该反应的平衡常数K=________(保留两位小数)。10-20min内,NO的平均反应速率为_______________;若30min后升高温度,达到新平衡时,容器中c(NO)∶c(N2) ∶c(CO2)=2∶1∶1,则该反应的ΔH________0(填“>”、“<”或“=”)。
②活性炭和铁屑混合可用于处理水中污染物。在相同条件下,测量总质量相同、铁的质量分数不同的铁炭混合物对水中Cu2+和Pb2+的去除率,结果如图所示。当混合物中铁的质量分数为0时,也能去除水中少量的Cu2+和Pb2+,其原因是_________________;当混合物中铁的质量分数大于50%时,随着铁的质量分数的增加,Cu2+和Pb2+的去除率不升反降,其主要原因是___________________________。
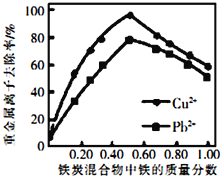
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中的溶质足量),当闭合该装置的电键K时,观察到电流表的指针发生了偏转。

请回答下列问题:
(1)甲池为_________(填“原电池”、“电解池”或“电镀池”),A电极的电极反应式为______。
(2)丙池中F电极为____(填“正极”、“负极”、“阴极”或“阳极”),该池总反应的方程式为_____。
(3)当乙池中C极质量减轻4.32g时,甲池中B电极理论上消耗O2的体积为_____mL(标准状况)。
(4)一段时间后,断开电键K。下列物质能使乙池恢复到反应前浓度的是______(填字母)。
A.Cu B.CuO C.Cu(OH)2 D.Cu(OH)2CO3
(5)甲醇和乙醇都可以做燃料。已知乙醇液体完全燃烧生成CO2气体和1mol液态水时放出热量453.3kJ,请写出乙醇燃烧的热化学方程式:____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据如图转化关系判断下列说法不正确的是(反应条件已略去)
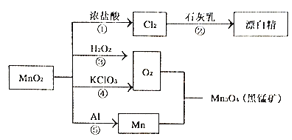
A. 反应①②③④⑤均属于氧化还原反应
B. 生成黑锰矿的反应中,3molMn参加反应转移4mol电子
C. 生成等量的O2,反应③和④转移的电子数之比为1:2
D. 反应⑤为铝热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在FeCl3、CuCl2和HCl的混合溶液中加入铁粉,待反应结束后,将剩余的固体滤出,发现固体能被磁铁吸引,则反应后溶液中大量存在的阳离子是( )
A.Cu2+和Fe2+
B.H+
C.Fe2+
D.Fe3+和Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
IVA 族元素及其化合物在材料等方面有重要用途。回答下列问题:
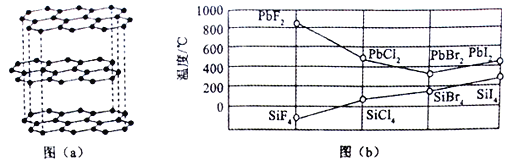
(1)碳的一种单质的结构如图(a)所示。该单质的晶体类型为________________,依据电子云的重叠方式,原子间存在的共价键类型有_____________,碳原子的杂化轨道类型为_________。
(2)石墨烯是从石墨材料中剥离出来的、由单层碳原子组成的二维晶体。将氢气加入到石墨烯中可制得一种新材料石墨烷。下列判断错误的是___________。
A.石墨烯是一种强度很高的材料
B.石墨烯是电的良导体而石墨烷则为绝缘体
C.石墨烯与石墨烷均为高分子化合物
D.石墨烯与H2 制得石墨烷的反应属于加成反应
(3)四卤化硅SiX4的沸点和二卤化铅PbX2 的熔点如图(b)所示。
①SiX4的沸点依F、Cl、Br、I 次序升高的原因是_________________________________。
②结合SiX4的沸点和PbX2的熔点的变化规律,可推断: 依F、Cl、Br、I 次序,PbX2 中的化学键的离子性___________、共价性______________。(填 “增 强”“不变”或“减 弱 ”)
(4)碳的另一种单质C60,晶胞结构与金属铜晶胞相似,其晶胞参数为a nm,晶体密度为_______g·cm-3(只列计算式,不需化简)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是SO2制取、性质检验、收集、尾气处理的装置,有关说法正确的是
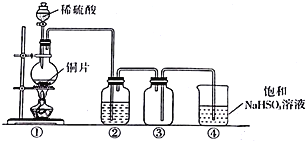
A. 上图中有两处错误
B. 装置①也可以用于制取氨气、氯气
C. 在②中加入品红或紫色石蕊试液都可以验证SO2的漂白性
D. 在②中加入BaCl2溶液,先生成白色沉淀,随后沉淀慢慢消失
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com