
 将盛有12mLNO2和O2混合气体的量筒倒立于水槽中,充分反应后,还剩余2mL无色气体,则原混合气体中O2的体积可能是( )
将盛有12mLNO2和O2混合气体的量筒倒立于水槽中,充分反应后,还剩余2mL无色气体,则原混合气体中O2的体积可能是( )| A、2.1mL | B、2.4mL |
| C、3.6mL | D、4mL |
| 1 |
| 3 |
| 1 |
| 3 |
| 4 |
| 5 |
| 1 |
| 5 |


科目:高中化学 来源: 题型:
| N2 | O2 | Ar | CO2 |
| -196°C | -183°C | -186°C | -78°C |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验事实 | 结论 | |
| ① | 将某气体通入品红溶液中,品红溶液褪色 | 该气体一定是SO2 |
| ② | 将燃烧的镁条放入CO2中能继续燃烧 | 还原性:Mg>C |
| ③ | NaHCO3溶液与Na[Al(OH)4]溶液混合产生白色沉淀 | 酸性:HCO3->Al(OH)3 |
| ④ | 常温下白磷可自燃而氮气须在放电时才与氧气反应 | 非金属性:P>N |
| ⑤ | 某无色晶体加入氢氧化钠浓溶液中并加热,产生的气体能使湿润红色石蕊试纸变蓝 | 该晶体中一定有NH4+ |
| A、②③⑤ | B、①②③ |
| C、③④⑤ | D、①③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、冰箱中使用的含氟制冷剂泄露后,会增加空气中的PM2.5 |
| B、浓硫酸具有强腐蚀性,可用浓硫酸刻蚀石英制艺术品 |
| C、施肥时,农家肥草木灰(有效成分K2CO3)不能与氮肥NH4Cl混合使用 |
| D、氯气和活性炭均可作为漂白剂,若同时使用,漂白效果会明显加强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
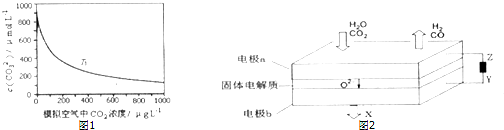
| ||
| 高温 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH4和C2H4 |
| B、CH4和C3H4 |
| C、C2H4和C3H4 |
| D、C2H2和C3H6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、柑橘属于碱性食品 |
| B、为防止流感传染,可将教室门窗关闭后,用食醋熏蒸,进行消毒 |
| C、氯化钠是家庭常用的防腐剂,可用来腌制食品 |
| D、棉、麻、丝、毛及合成纤维完全燃烧都只生成CO2和H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、由MgCl2制取Mg是放热过程 |
| B、热稳定性:MgI2>MgBr2>MgCl2>MgF2 |
| C、常温下氧化性:F2<Cl2<Br2<I2 |
| D、由图可知此温度下MgBr2(s)与Cl2(g)反应的热化学方程式为:MgBr2(s)+Cl2(g)═MgCl2(s)+Br2(g),△H=-117kJ?mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com