
下列说法正确的是
A.增大反应物浓度,可增大单位体积内活化分子的百分数,从而使有效碰撞次数增加
B.对于有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增大活化分子的百分数,从而使反应速率增大
C.改变条件能使化学反应速率增大的主要原因是增大了反应物分子中活化分子的有效碰撞几率
D.对于本来不能发生的化学反应,改变条件可以使反应发生
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2016-2017学年广西省高一上9月月考化学试卷(解析版) 题型:选择题
下列可以大量共存且溶液是无色的离子组是( )
A.NO3-、SO42-、K+、Mg2+ B.Ba2+、Mg2+、 Cl-、SO42-
C.H+、K+、OH-、NO3- D.H+、Na+、NO3-、Cu2+
查看答案和解析>>
科目:高中化学 来源:2016-2017学年宁夏高一上学期期中化学卷(解析版) 题型:选择题
某氯化镁溶液的密度为1.18 g/cm,其中镁离子的质量分数为5.1%。300 mL该溶液中Cl-的物质的量约为( )
A.0.37 mol B.0.63 mol C.0.74 mol D.1.5 mol
查看答案和解析>>
科目:高中化学 来源:2016-2017学年宁夏高二上学期期中化学卷(解析版) 题型:填空题
为探究用CO2来生产燃料甲醇的反应原理,现进行如下实验:在体积为1 L的密闭容器中,充入1 mol CO2和3 molH2,一定条件下发生反应:CO2(g)+3H2(g)  CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1,T温度下,测得CO2和CH3OH(g)的浓度随时间变化如下图
CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1,T温度下,测得CO2和CH3OH(g)的浓度随时间变化如下图 。请回答下列问题:
。请回答下列问题:

(1) 达平衡时,氢气的平衡浓度为C(H2)= 。
(2) 能够说明该反应已达到平衡的是 (填字母序号,下同)。
A.恒温、恒容时,容器内的压强不再变化
B.恒温、恒容时,容器内混合气体的密度不再变化
C.一定条件下,CO、H2和CH3OH的浓度保持不变
D.一定条件下,单位时间内消耗3 mol H2的同时生成1 mol CH3OH
(3)下列措施中能使平衡混合物中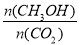 增大的是______________。
增大的是______________。
A.加入催化剂 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离 D.降低温度
(4) 求此温度(T)下该反应的平衡常数K = 。若开始时向该1 L密闭容器中充入1 mol CO2,2molH2,1.5mol CH3OH和1 mol H2O(g),则反应向 (填“正”或“逆”)反应方向进行。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年宁夏高二上学期期中化学卷(解析版) 题型:选择题
下列关于焓判据和熵判据的说法中,不正确的是
A.放热的自发过程可能是熵减小的过程,吸热的自发过程一定为熵增加的过程
B.由焓判据和熵判据组合成的复合判据,将更适合于所有的过程
C.在室温下碳酸钙的分解反应不能自发进行,但同样是这个吸热反应在较高温度(1200 K)下则能自发进行
D.放热过程(ΔH<0)或熵增加(ΔS>0)的过程一定是自发的
查看答案和解析>>
科目:高中化学 来源:2016-2017学年宁夏高二上学期期中化学卷(解析版) 题型:选择题
通常人们把拆开1 mol某化学键所吸收的能量或形成1 m ol某化学键所释放的能量看作该化学键的键能,键能的大小可用于估算化学反应的反应热(ΔH),已知
ol某化学键所释放的能量看作该化学键的键能,键能的大小可用于估算化学反应的反应热(ΔH),已知
化学健 | H-H | Cl-Cl | H-Cl |
键能 | 436 kJ/mol | 243 kJ/mol | 431 kJ/mol |
则下列热化学方程式不正确的是
A.1/2 H2(g)+1/2Cl2(g)=HCl(g) ΔH=-91.5 kJ·mol-1
B.H2(g)+Cl2(g)=2HCl(g) ΔH=-183 kJ·mol-1
C.2HCl(g)=H2(g)+Cl2(g) ΔH=+183 kJ·mol-1
D.1/2 H2(g)+1/2Cl2(g)=HCl(g) ΔH=+91.5 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年宁夏高二上学期期中化学卷(解析版) 题型:选择题
下列与化学反应能量变化相关的叙述正确的是
A.生成物总能量一定低于反应物总能量
B.放热反应的反应速率总是大于吸热反应的反应速率
C.应用盖斯定律,可计算某些难以直接测量的反应焓变
D.同温同 压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H不同
压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H不同
查看答案和解析>>
科目:高中化学 来源:2016-2017学年内蒙古高二上10月月考化学卷(解析版) 题型:选择题
常温下,0.1mol/L的三种盐溶液NaX、NaY、NaZ的pH分别为7、8、9,则下列说法正确的是
A.HX是弱酸 B.离子浓度:c(Z-)>c(Y-)>c(X-)
C.电离常数:K(HZ)>K(HY) D.c(X-)=c(Y-)+c(HY)=c(Z-)+c(HZ)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西大学附中高一上10月模块诊断化学卷(解析版) 题型:选择题
VmLAl2(SO4)3 溶液中含Al3+ag,取V/4mL溶液稀释到4VmL,则稀释后溶液中SO42-的物质的量浓度是
A.125a/36V mol/L B.125a/18Vmol/L
C.125a/9V mol/L D.125a/54V mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com