
(13分)碳、氮、氧、氟都是位于第二周期的重要的非金属元素。请回答下列问题:
(1)基态氟原子的核外电子排布式是______________ 。
(2)C、N、O、F四种元素第一电离能从大到小的顺序是_________________。
(3)①碳和另外三种元素均可形成化合物。四氟化碳的空间构型为____________,CF4可以利用甲烷与Cl2和HF在一定条件下反应来制备,其反应化学方程式为__ __ ___。
②CO是__________分子(填“极性”或“非极性”),CO的常见等电子体为N2、CN-,已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为___________。
③C3N4是一种新型材料,它的硬度比金刚石还高,可做切割工具,可推测出C3N4属于_________晶体。
(4)N4分子结构和白磷一样都是正四面体。又已知断裂1molN-N键吸收167kJ热量,生成1 molN≡N键放出942kJ热量,0.1 molN4转变为N2将放出____________热量:
(5)CaF2和CaC2都属于离子晶体。CaF2晶体的密度为a g·cm-3,则晶胞(如图)的体积是_______________(只要求列出算式)。

(6)CaC2晶体的晶胞与氯化钠相似,但由于CaC2晶体中的C22-存在,使晶胞沿一个方向拉长,则CaC2晶体中1个C22-周围距离最近且相等的Ca2+数目为__________,C22-与O22+ 互为等电子体,O22+的电子式为____________。
(1)1s22s22p5 (2)F>N>O>C
(3)①正四面体 CH4 + 4 Cl2 + 4 HF  CF4 + 8 HCl (2分)
CF4 + 8 HCl (2分)
②极性 1:1(或2:2) ③ 原子
(4)88.2 kJ (5)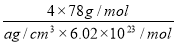 (2分)
(2分)
(6)4 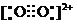
【解析】
试题分析:(1)F为9号元素核外有9个电子,根据构造原理其电子排布式为:1s22s22p5。
(2)同一周期元素中,元素的第一电离能随着原子序数的增大而呈增大趋势,但第IIA族、第VA族元素的第一电离能大于相邻元素,这几种元素都是第二周期元素,它们的族序数分别是:第IVA族、第VA族、第VIA族、第VIIA族,所以它们的第一电离能大小顺序是F>N>O>C。
(3)①四氟化碳与甲烷的空间构型相同,所以四氟化碳的空间构型为正四面体;甲烷与Cl2和HF反应生成四氟化碳,其反应的化学方程式为:CH4 + 4 Cl2 + 4 HF  CF4 + 8 HCl。
CF4 + 8 HCl。
②CO中C原子与O原子间形成的共价键为极性键,CO为直线分子,所以CO为极性分子;CN-与N2结构相似,C原子与N原子之间形成三键,则HCN分子结构式为H-C≡N,三键中含有1个σ键、2个π键,单键属于σ键,故HCN分子中σ键与π键数目之比为1:1。
③C3N4是一种新型材料,它的硬度比金刚石还高,具有原子晶体的物理性质,所以属于原子晶体。
(4)由题意知,N≡N的键能为942kJ/mol,N-N键的键能为167kJ/mol,生成1molN4的反应为:2N2(g)=N4(g),反应热等于反应物的总键能减去生成物的总键能,故反应热△H=2×942kJ/mol-6×167kJ/mol=+882kJ/mol,所以0.1molN4转变为N2将放出88.2kJ热量。
(5)在晶胞中Ca2+数目为8×1/8+6×1/2=4,F-数目为8,则V=m÷ρ=4×78g/mol÷(ag?cm-3×6.02×1023mol-1)=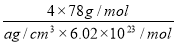 。
。
(6)氯化钠晶胞中配位数为6,每个阴离子周围距离最近且相等的阳离子数目为6,由于CaC2晶体中的C22-存在,使晶胞沿一个方向拉长,则CaC2晶体中1个C22-周围距离最近且相等的Ca2+数目减少,为4个;根据等电子体的结构相似,则O22+的电子式 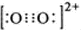 。
。
考点:本题考查原子核外电子排布、元素电离能、电负性的含义及应用、“等电子原理”的应用、晶胞的计算、反应热和焓变。


 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案科目:高中化学 来源:2015届北京市朝阳区高三年级第一学期期中统一考试化学试卷(解析版) 题型:选择题
重水(2H2O)是重要的核工业原料,下列说法不正确的是
A.氘( )原子核内有1个质子
)原子核内有1个质子
B.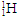 与
与 是不同的核素
是不同的核素
C.1H2O与2H2O是同一种物质
D.1H218O与2H216O的相对分子质量相同
查看答案和解析>>
科目:高中化学 来源:2015届内蒙古赤峰市高三上学期9月质量检测化学试卷(解析版) 题型:选择题
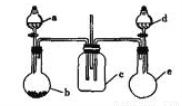
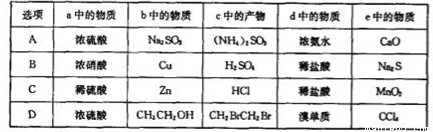
实验室某些物质的制备装置如图所示(省略夹持装置和净化装置),仅用此装置和表中提供的物质完成相关实验,最合理的是
查看答案和解析>>
科目:高中化学 来源:2015届内蒙古赤峰市宁城县高三上学期摸底统一考试化学试卷(解析版) 题型:选择题
据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如下图所示。
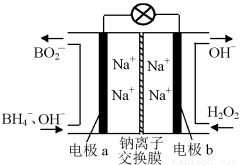
下列说法错误的是( )
A.电池放电时Na+从a极区移向b极区
B.电极b采用MnO2,MnO2既作电极材料又有催化作用
C.该电池的负极反应为:BH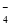 +8OH--8e-=BO
+8OH--8e-=BO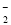 +6H2O
+6H2O
D.每消耗3 mol H2O2,转移的电子为3 mol
查看答案和解析>>
科目:高中化学 来源:2015届内蒙古赤峰市宁城县高三上学期摸底统一考试化学试卷(解析版) 题型:选择题
下列化合物的一氯代物的数目排列顺序正确的是( )
①CH3CH2CH2CH2CH2CH3 ②(CH3)2CHCH(CH3)2
③(CH3)3CCH2CH3 ④(CH3) 3CC(CH3) 3
A.①>②>③>④ B.②>③=①>④
C.③>②>④>① D.③=①>②>④
查看答案和解析>>
科目:高中化学 来源:2015届内蒙古巴彦淖尔市高三10月月考化学试卷(解析版) 题型:选择题
已知下列热化学方程式:
Zn(s)+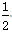 O2(g)===ZnO(s) ΔH1=-351.1 kJ/mol
O2(g)===ZnO(s) ΔH1=-351.1 kJ/mol
Hg(l)+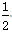 O2(g)===HgO(s) ΔH2=-90.7 kJ/mol
O2(g)===HgO(s) ΔH2=-90.7 kJ/mol
由此可知Zn(s)+HgO(s)===ZnO(s)+Hg( l) ΔH3,其中ΔH3是
A.-441.8 kJ/mol B.-254.6 kJ/mol
C.-260.4 kJ/mol D.-438.9 kJ/mol
查看答案和解析>>
科目:高中化学 来源:2015届内蒙古高二下学期期末考试化学试卷(解析版) 题型:填空题
(普通班)(12分)咖啡酸具有止血、镇咳、祛痰等疗效,其结构为

(1)咖啡酸分子中的含氧官能团有 ;
(2)有关咖啡酸性质的叙述错误的是 ;
A.在浓硫酸、加热条件下能发生消去反应
B.既能和浓溴水发生加成反应也能发生取代反应
C.能与酸性高锰酸钾溶液反应
D.1mol 咖啡酸在一定条件下能与4molH2发生加成反应
(3)有机物A(分子式为C11H12O4)在一定条件下能发生如下转化:

①D、E的结构简式分别为 、 ;
②B→C反应的化学方程式为 ;
(4)R是咖啡酸的同分异构体,具有如下特点:①R具有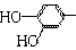 结构;②能发生水解反应;R的结构简式为 (任写1种)。
结构;②能发生水解反应;R的结构简式为 (任写1种)。
查看答案和解析>>
科目:高中化学 来源:2014~2015江苏省高一上学期期中化学试卷(解析版) 题型:选择题
某物质灼烧时,焰色为黄色,下列判断中正确的是
A.该物质一定是钠的化合物
B.该物质一定含钠元素
C.能确定该物质中一定不含钾元素
D.该物质一定是金属钠
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com