
| A. | ①②③ | B. | ①③④ | C. | ①② | D. | ①③ |
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案科目:高中化学 来源: 题型:选择题
| A. | 298 K时,加蒸馏水稀释HF溶液,$\frac{c({F}^{-})}{c(HF)}$保持不变 | |
| B. | 308 K时,HF的电离常数Ka>3.5×10-4 | |
| C. | 298 K时,向饱和CaF2溶液中加入少量CaCl2,Ksp(CaF2)会减小 | |
| D. | 2HF(aq)+Ca2+(aq)?CaF2(s)+2H+(aq) K≈0.68 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 44.Og14CO2与14N2O的混合物中所含中子数为22NA | |
| B. | 标准状况下,2.24L甲醛所含o键数目为0.3NA | |
| C. | 常温常压下,4.5gH2O与足量Na2O2反应转移的电子数目为0.5 NA | |
| D. | 50mL 18mol/L硫酸与足量Cu共热,转移的电子数为0.9NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
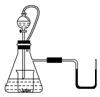 如图所示,若锥形瓶内是水,分液漏斗内的液体也是水,向烧杯内滴加水时,发现U形管内液体慢慢右移,恢复到原温度后液面左边与右边基本相平,则下列说法正确的是( )
如图所示,若锥形瓶内是水,分液漏斗内的液体也是水,向烧杯内滴加水时,发现U形管内液体慢慢右移,恢复到原温度后液面左边与右边基本相平,则下列说法正确的是( )| A. | U型管内液体慢慢向右移动说明将分液漏斗中的水滴入到烧杯中一定发生了化学反应 | |
| B. | U型管内液体慢慢向右移动是由于锥形瓶中气体的总物质的量增大造成压强增大而引起 | |
| C. | 该装置中连接分液漏斗和锥形瓶的橡胶管对于上述实验现象而言其实是可有可无的 | |
| D. | 小烧杯中的物质可以是NaOH也可以是Na2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O | |
| B. | 由水电离出的c(OH-)=1×10-12mol/L的溶液中可能大量存在K+、I-、Mg2+、NO3- | |
| C. | 向NH4Al(SO4)2溶液中滴加Ba(OH)2溶液使SO42-完全沉淀:NH4++Al3++2SO42-+2Ba2++4OH-=NH3•H2O+Al(OH)3↓+2BaSO4↓ | |
| D. | 标准状况下,将1.12LCO2气体通入1L0.1mol/L的KAlO2溶液中:CO2+2H2O+AlO2-=Al(OH)3↓+HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:2 | B. | 2:1 | C. | 2:5 | D. | 5:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .我们还学习了与乙醇结构相似的一系列有机物如:
.我们还学习了与乙醇结构相似的一系列有机物如:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com